题目内容
10.下列说法正确的是( )| A. | 增大反应物浓度可以增大活化分子百分数,从而使反应速率增大 | |
| B. | 汽车尾气的催化转化装置可将尾气中的NO和CO等有害气体快速地转化为N2和CO2,其原因是催化剂可增大NO和CO反应的活化能 | |
| C. | 常温下,反应C(s)+CO2(g)═2CO(g)不能自发进行,则该反应的△H>0 | |
| D. | 在“中和热的测量实验”中测定反应后温度的操作方法:将量筒中的NaOH溶液经玻璃棒引流缓缓倒入盛有盐酸的简易量热计中,立即盖上盖板,并用环形玻璃搅拌棒不断搅拌,准确读出并记录反应体系的最高温度 |
分析 A.增大浓度,活化分子百分数不变;
B.加入催化剂,降低反应的活化能;
C.如能自发进行,应满足△H-T•△S<0;
D.应迅速将氢氧化钠溶液倒入.
解答 解:A.增大浓度,单位体积的活化分子数目增多,但活化分子百分数不变,故A错误;
B.加入催化剂,降低反应的活化能,故B错误;
C.△S>0,该反应不能自发进行,说明△H-T•△S>0,则△H>0,故C正确;
D.实验时为避免热量损失,应迅速将氢氧化钠溶液倒入,故D错误.
故选C.
点评 本题综合考查化学反应与能量变化,反应速率的影响因素、中和热的测定等知识,为高考常见题型和高频考点,侧重考查学生的分析能力和实验能力,难度不大.

练习册系列答案
相关题目
1.下列有关物质的性质或应用的说法正确的是( )
| A. | 用核磁共振氢谱鉴别1-丙醇和2-丙醇 | |
| B. | 用酸性KMnO4溶液除去乙烷中混有的乙烯 | |
| C. | 间二溴苯仅有一种空间结构可证明苯分子中不存在单双键交替的结构 | |
| D. | 甲烷、乙烯和苯在工业上都可通过石油分馏得到 |
18.已知相同条件下,下列反应的焓变和乎衡常数分别表示为:
①2H2O(g)=O2(g)+2H2(g)△H1 K1=x
②Cl2(g)+H2(g)=2HCl(g)△H2 K2=y
③2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)△H3 K3=x
则下列关系正确的是( )
①2H2O(g)=O2(g)+2H2(g)△H1 K1=x
②Cl2(g)+H2(g)=2HCl(g)△H2 K2=y
③2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)△H3 K3=x
则下列关系正确的是( )
| A. | △H3=△H1+2△H2 x=xy2 | B. | H3=△H1+△H2 z=x+y | ||
| C. | H3=△H1+2△H2 x=x-y2 | D. | H3=△H1+△H2 z=$\frac{x}{y}$ |
5.化学反应速率是化学反应原理的重要组成部分.请回答下列问题:
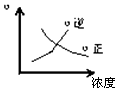
(1)已知一定条件下发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,在反应过程中,正反应速率的变化如图所示,请根据速率的变化回答采取的措施(改变的条件).

(2)探究反应条件对0.l0mol/L,Na2S2O3溶液与稀H2SO4反应速率的影响.其设计与测定结果如表:
上述实验①③是探究温度对化学反应速率的影响;若上述实验①②是探究浓度对化学反应速率的影响,则表格中“甲”为V(蒸馏水)/mL,a为5.0;乙是实验需要测量的物理量,则表格中“乙”为出现浑浊的时间/min.
(3)已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在开始一段时间内,反应速率较小,溶液褪色不明显;但不久突然褪色,反应速率明显增大.
①针对上述现象,某同学认为该反应放热,导致溶液温度上升,反应速率增大.从影响化学反应速率的因素看,你猜想还可能是催化剂(或锰离子的催化作用)的影响.
②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,可以在反应一开始时加入C(填字母序号).
A.硫酸钾B.氯化锰c.硫酸锰D.水.
(1)已知一定条件下发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,在反应过程中,正反应速率的变化如图所示,请根据速率的变化回答采取的措施(改变的条件).

(2)探究反应条件对0.l0mol/L,Na2S2O3溶液与稀H2SO4反应速率的影响.其设计与测定结果如表:
| 编号 | 反应温度/℃ | Na2S2O3浓液/mL | 甲 | 0.1mol/LH2SO4溶液/mL | 乙 |
| ① | 25℃ | 10.0 | 0 | 10.0 | |
| ② | 25℃ | 5.0 | a | 10.0 | |
| ③ | 45℃ | 10.0 | 0 | 10.0 |
(3)已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在开始一段时间内,反应速率较小,溶液褪色不明显;但不久突然褪色,反应速率明显增大.
①针对上述现象,某同学认为该反应放热,导致溶液温度上升,反应速率增大.从影响化学反应速率的因素看,你猜想还可能是催化剂(或锰离子的催化作用)的影响.
②若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,可以在反应一开始时加入C(填字母序号).
A.硫酸钾B.氯化锰c.硫酸锰D.水.
2.请回答下列问题:
(1)纯水在T℃时,pH=6,该温度下1mol•L-1的NaOH溶液中,由水电离出的c(OH-)=10-12 mol•L-1.
(2)某一元弱酸溶液(A)与二元强酸(B)的pH相等.若将两溶液稀释相同的倍数后,pH(A)<pH(B) (填“>”、“=”或“<”).现用上述稀释溶液中和等浓度等体积的NaOH溶液,则需稀释溶液的体积V(A)<V(B)(填“>”、“=”或“<”).
(3)已知:二元酸H2R 的电离方程式是:H2R=H++HR-,HR-?R2-+H+,若0.1mol•L-1NaHR溶液的c(H+)=a mol•L-1,则0.1mol•L-1H2R溶液中c(H+)< (0.1+a) mol•L-1(填“<”、“>”或“=”),理由是H2R中第一步电离出的H+对HR-的电离产生了抑制作用.
(4)电离平衡常数是衡量弱电解质电离程度的物理量.已知:
①25℃时,有等浓度的HCN溶液、H2CO3溶液和CH3COOH溶液,三溶液的pH由大到小的顺序为H2CO3>HCN>CH3COOH(用化学式表示).
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为NaCN+H2O+CO2=HCN+NaHCO3.
(1)纯水在T℃时,pH=6,该温度下1mol•L-1的NaOH溶液中,由水电离出的c(OH-)=10-12 mol•L-1.
(2)某一元弱酸溶液(A)与二元强酸(B)的pH相等.若将两溶液稀释相同的倍数后,pH(A)<pH(B) (填“>”、“=”或“<”).现用上述稀释溶液中和等浓度等体积的NaOH溶液,则需稀释溶液的体积V(A)<V(B)(填“>”、“=”或“<”).
(3)已知:二元酸H2R 的电离方程式是:H2R=H++HR-,HR-?R2-+H+,若0.1mol•L-1NaHR溶液的c(H+)=a mol•L-1,则0.1mol•L-1H2R溶液中c(H+)< (0.1+a) mol•L-1(填“<”、“>”或“=”),理由是H2R中第一步电离出的H+对HR-的电离产生了抑制作用.
(4)电离平衡常数是衡量弱电解质电离程度的物理量.已知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为NaCN+H2O+CO2=HCN+NaHCO3.
15.下列离子方程式正确的是( )
| A. | 氧化铁和盐酸:O2-+2H+═H2O | |
| B. | 向澄清石灰水中通入过量的CO2:Ca2++2OH-+CO2═CaCO3↓+H2O | |
| C. | 澄清石灰水和Ca(HCO3)2溶液反应:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| D. | 氢氧化钡溶液和硫酸镁溶液反应:Ba2++SO42-═BaSO4↓ |
16.用胆矾配制0.2mol/L的CuSO4溶液,下列操作正确的是( )
| A. | 取50g胆矾溶于1L水中 | B. | 取50g胆矾溶于水配成1L溶液 | ||
| C. | 取32g胆矾溶于水配成1L溶液 | D. | 取无水硫酸铜32g溶于1L水中 |