题目内容
15.对于可逆反应 2AB3(g)?A2(g)+3B2(g)△H>0下列图象正确的是( )| A. | 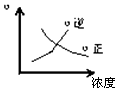 | B. | 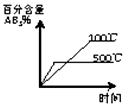 | C. | 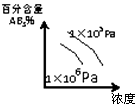 | D. |  |
分析 该反应是一个反应前后气体体积增大的吸热反应,
A.反应达到平衡状态时,增大浓度,正逆反应速率都增大;
B.该反应的正反应是吸热反应,升高温度平衡正向移动;
C.相同浓度条件下,该反应前后气体体积减小,增大压强平衡逆向移动;
D.压强相同的条件下,升高温度平衡正向移动.
解答 解:A.正逆反应速率相等时该反应达到平衡状态,增大物质浓度,正逆反应速率都增大,图象不符合,故A错误;
B.该反应的正反应是吸热反应,升高温度平衡正向浓度,则AB3的含量减小,符合图象,故B正确;
C.相同浓度条件下,该反应前后气体体积减小,增大压强平衡逆向移动,则AB3的含量增大,不符合图象,故C错误;
D.压强相同的条件下,升高温度平衡正向移动,则AB3的含量减小,不符合图象,故D错误;
故选B.
点评 本题考查图象分析,为高频考点,侧重考查学生图象分析、比较、判断能力,明确方程式特点及反应物与温度、压强的关系是解本题关键,注意CD采用“定一议二”的方法解答,题目难度不大.

练习册系列答案
相关题目
5.下列对于“摩尔”的理解不正确的是( )
| A. | 摩尔是一个物理量 | |
| B. | 摩尔是物质的量的单位,简称摩,符号为mol | |
| C. | 1mol12C与0.012kg12C所含碳原子数相同 | |
| D. | 1molO2约含6.02×1023个氧分子 |
6.以石化产品乙烯、丙烯为原料合成厌氧胶的流程如图.

关于该过程的相关叙述正确的是( )

关于该过程的相关叙述正确的是( )
| A. | 反应④的反应类型是加聚 | B. | 物质A含有两种官能团 | ||
| C. | 物质B催化氧化后可以得到乙醛 | D. | 1mol物质D最多可以消耗2molNaOH |
3.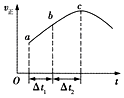 向绝热恒容密闭容器中通入CO和H2O(g),在一定条件下使反应CO(g)+H2O(g)?CO2(g)+H2(g)达到判平衡,正反应速率随时间变化的示意图如图所示.由图可得出的正确结论是( )
向绝热恒容密闭容器中通入CO和H2O(g),在一定条件下使反应CO(g)+H2O(g)?CO2(g)+H2(g)达到判平衡,正反应速率随时间变化的示意图如图所示.由图可得出的正确结论是( )
 向绝热恒容密闭容器中通入CO和H2O(g),在一定条件下使反应CO(g)+H2O(g)?CO2(g)+H2(g)达到判平衡,正反应速率随时间变化的示意图如图所示.由图可得出的正确结论是( )
向绝热恒容密闭容器中通入CO和H2O(g),在一定条件下使反应CO(g)+H2O(g)?CO2(g)+H2(g)达到判平衡,正反应速率随时间变化的示意图如图所示.由图可得出的正确结论是( )| A. | 反应物的总能量低于生成物的总能量 | |
| B. | △t1=△t2时,CO的转化率:a~b段小于b〜c段 | |
| C. | 反应在c点达到平衡状态 | |
| D. | 反应物浓度:a点小于b点 |
10.下列说法正确的是( )
| A. | 增大反应物浓度可以增大活化分子百分数,从而使反应速率增大 | |
| B. | 汽车尾气的催化转化装置可将尾气中的NO和CO等有害气体快速地转化为N2和CO2,其原因是催化剂可增大NO和CO反应的活化能 | |
| C. | 常温下,反应C(s)+CO2(g)═2CO(g)不能自发进行,则该反应的△H>0 | |
| D. | 在“中和热的测量实验”中测定反应后温度的操作方法:将量筒中的NaOH溶液经玻璃棒引流缓缓倒入盛有盐酸的简易量热计中,立即盖上盖板,并用环形玻璃搅拌棒不断搅拌,准确读出并记录反应体系的最高温度 |
20.α1和α2,c1和c2分别为两个恒容容器中平衡体系N2O4(g)?2NO2(g)和3O2(g)?2O3(g)的反应物转化率及反应物的平衡浓度,在温度不变的情况下,均增加反应物的物质的量,下列判断正确的是( )
| A. | α1、α2均减小,c1、c2均增大 | B. | α1、α2均增大,c1、c2均减小 | ||
| C. | α1减小,α2增大,c1、c2均增大 | D. | α1减小,α2增大,c1增大,c2减小 |
3.如图1,科学研究表明,当前应用最广泛的化石燃料到本世纪中叶将枯竭,解决此危机的唯一途径是实现燃料和燃烧产物之间的良性循环:
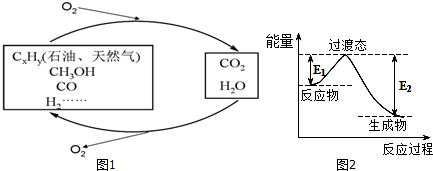
(1)一种常用的方法是在230℃、有催化剂条件下将CO2和H2转化为甲醇蒸汽和水蒸气.图2是生成1molCH3OH时的能量变化示意图.
已知破坏1mol不同共价键的能量(kJ)分别是:
已知E1=8.2kJ•mol-1,则E2=198.8kJ•mol-1.
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如下三组数据:
①该反应的△H<0(填“<”或“>”).
②实验2条件下的平衡常数K=$\frac{1}{3}$.
③实验3中,若平衡时H2O的转化率为25%,则$\frac{a}{b}$=0.5.
④实验4,若900℃时,在容器中加入CO、H2O、CO2、H2各1mol,则此时V正<V逆(填“<”或“>”或“=”).
(3)捕捉CO2可以利用Na2CO3溶液.先用Na2CO3溶液吸收CO2生成NaHCO3,然后使NaHCO3分解,Na2CO3可以进行循环使用.将100mL 0.1mol/LNa2CO3的溶液中通入112mL(已换算为标准状况)的CO2,溶液中没有晶体析出,则:
①反应后溶液中的各离子浓度由大到小的顺序是c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
②反应后的溶液可以作“缓冲液”(当往溶液中加入一定量的酸和碱时,有阻碍溶液pH变化的作用),请解释其原理反应后的溶液存在HCO3-?CO32-+H+,加入少量的酸,平衡逆向移动,溶液pH变化不大;加入少量的碱平衡正向移动,溶液pH变化也不大,故该溶液可以作“缓冲液”.

(1)一种常用的方法是在230℃、有催化剂条件下将CO2和H2转化为甲醇蒸汽和水蒸气.图2是生成1molCH3OH时的能量变化示意图.
已知破坏1mol不同共价键的能量(kJ)分别是:
| C-H | C-O | C=O | H-H | H-O |
| 413.4 | 351 | 745 | 436 | 462.8 |
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如下三组数据:
| 实验 | 温度/℃ | 起始量] | 达到平衡 | |||
| CO/mol | H2O/mol | H2/mol | CO转化率 | 所需时间/min | ||
| 1 | 650 | 4 | 2 | 1.6 | 6 | |
| 2 | 900 | 2 | 1 | 25% | 3 | |
| 3 | 900 | a | b | c | t | |
②实验2条件下的平衡常数K=$\frac{1}{3}$.
③实验3中,若平衡时H2O的转化率为25%,则$\frac{a}{b}$=0.5.
④实验4,若900℃时,在容器中加入CO、H2O、CO2、H2各1mol,则此时V正<V逆(填“<”或“>”或“=”).
(3)捕捉CO2可以利用Na2CO3溶液.先用Na2CO3溶液吸收CO2生成NaHCO3,然后使NaHCO3分解,Na2CO3可以进行循环使用.将100mL 0.1mol/LNa2CO3的溶液中通入112mL(已换算为标准状况)的CO2,溶液中没有晶体析出,则:
①反应后溶液中的各离子浓度由大到小的顺序是c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
②反应后的溶液可以作“缓冲液”(当往溶液中加入一定量的酸和碱时,有阻碍溶液pH变化的作用),请解释其原理反应后的溶液存在HCO3-?CO32-+H+,加入少量的酸,平衡逆向移动,溶液pH变化不大;加入少量的碱平衡正向移动,溶液pH变化也不大,故该溶液可以作“缓冲液”.
20.一定温度、压强下,若一个氦原子实际质量是b g,12C的原子实际质量是a g,氦气的密度为ρ g/cm3,该温度压强下氦气的摩尔体积为Vm L/mol,NA是阿伏加德罗常数的值,下列说法正确的是( )
| A. | 氦原子的相对原子质量是$\frac{12a}{b}$ | B. | 氦气的摩尔质量是(ρVm) g/mol | ||
| C. | m g氦气所含质子数是$\frac{2m}{b}$ | D. | m g氦气的物质的量是$\frac{m}{(b{N}_{A})}$ |
1.下列对对应现象的描述与离子方程式都正确的是( )
| A. | 金属镁与稀盐酸反应:有气体生成,Mg+2 H++2Cl-═MgCl2+H2↑ | |
| B. | 氯化钡溶液与硫酸反应:有白色沉淀生成:SO42-+Ba2+═BaSO4↓ | |
| C. | 碳酸钠溶液与盐酸反应:有气泡逸出:Na2CO3+2 H+═2Na++CO2↑+H2O | |
| D. | 过量铁粉与氯化铜溶液反应:溶液由蓝色变成浅绿色,同时有红色固体生成:Fe+Cu2+═Fe3++Cu |