题目内容
9.能正确表示下列反应的离子方程式是( )| A. | 向Fe(NO3)2稀溶液中加入盐酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O | |
| B. | 铝和氢氧化钠水溶液反应:Al+2OH-+2H2O═AlO2-+3H2↑ | |
| C. | 碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH4++OH- $\frac{\underline{\;△\;}}{\;}$NH3↑+H2O | |
| D. | AlCl3溶液中滴加足量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
分析 A.发生氧化还原反应,遵循电子、电荷守恒;
B.电子、电荷不守恒;
C.漏写碳酸氢根离子与碱的反应;
D.反应生成氢氧化铝和氯化铵.
解答 解:A.向Fe(NO3)2稀溶液中加入盐酸的离子反应为3Fe2++4H++NO3-═3Fe3++NO↑+2H2O,故A正确;
B.铝和氢氧化钠水溶液反应的离子反应为2Al+2OH-+2H2O═2AlO2-+3H2↑,故B错误;
C.碳酸氢铵溶液与足量的NaOH溶液混合后加热的离子反应为HCO3-+NH4++2OH- $\frac{\underline{\;△\;}}{\;}$NH3↑+2H2O+CO32-,故C错误;
D.AlCl3溶液中滴加足量氨水的离子反应为A13++3NH3•H2O=Al(OH)3↓+3NH4+,故D错误;
故选A.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
相关题目
16.除去下列物质中的少量杂质(括号内的物质为杂质),所选用的试剂或方法不正确的是( )
| A. | CO2(SO2):饱和Na2CO3溶液 | B. | NO(NO2):水 | ||
| C. | Cl2(HCl):饱和NaCl溶液 | D. | Na2CO3固体(NaHCO3):加热 |
17.下列说法错误的是( )
| A. | 胶体粒子的大小在1nm~1000nm之间 | |
| B. | 向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体 | |
| C. | 明矾在水中能生成氢氧化铝胶体,故可作净水剂 | |
| D. | 用光束照射CuSO4溶液不能观察到丁达尔效应 |
14.某同学配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
| A. | 所用NaOH已经潮解 | |
| B. | 定容时观察液面俯视 | |
| C. | 洗涤烧杯和玻棒的溶液未转入容量瓶中 | |
| D. | 用带游砝的托盘天平称2.4 g NaOH时误用了“左码右物”方法 |
4.下列做法不利于金属防护的是( )
| A. | 切菜刀切菜后不洗净就放回刀架 | B. | 将钢铁制成不锈钢 | ||
| C. | 在铁塔的表面喷漆 | D. | 埋在地下的钢管与锌块连接 |
14.Cl2是纺织工业常用的漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”.S2O32-和 Cl2反应的2-产物之一为 SO42-下列说法不正确的是( )
| A. | 该反应中的还原剂是 S2O32- | |
| B. | 根据该反应可判断氧化性:Cl2>SO42- | |
| C. | 上述反应中,每生成 1 mol SO42-,可脱去2molCl2 | |
| D. | 该反应的氧化产物是 Cl- |
18.下列各组物质熔点比较,不正确的是( )
| A. | 金刚石>晶体硅 | B. | NaCl>金刚石 | C. | MgO>l2 | D. | CO2<SiO2 |
19.下列说法正确的是( )
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 不需加热就能发生的反应一定是放热反应 | |
| C. | 反应物总能量高于生成物总能量的反应一定是放热反应 | |
| D. | 破坏反应物中的化学键所吸收的总能量多于形成生成物中化学键所放出的总能量的反应一定是放热反应 |
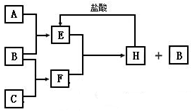 A、B、C是按原子序数由小到大排列的第二、三周期元素的单质.B、E均为组成空气的成分.F的焰色反应呈黄色.在一定条件下,各物质之间的相互转化关系如图(图中部分产物未列出):
A、B、C是按原子序数由小到大排列的第二、三周期元素的单质.B、E均为组成空气的成分.F的焰色反应呈黄色.在一定条件下,各物质之间的相互转化关系如图(图中部分产物未列出):