题目内容
14.某同学配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )| A. | 所用NaOH已经潮解 | |
| B. | 定容时观察液面俯视 | |
| C. | 洗涤烧杯和玻棒的溶液未转入容量瓶中 | |
| D. | 用带游砝的托盘天平称2.4 g NaOH时误用了“左码右物”方法 |
分析 结合c=$\frac{n}{V}$可知,V偏小或n偏大,则导致所配溶液浓度偏高,以此来解答.
解答 解:A.所用NaOH已经潮解,称量NaOH的质量偏小,则n偏小,浓度偏小,故A不选;
B.定容时观察液面俯视,V偏小,则所配溶液浓度偏高,故B选;
C.洗涤烧杯和玻棒的溶液未转入容量瓶中,n偏小,浓度偏小,故C不选;
D.用带游砝的托盘天平称2.4 g NaOH时误用了“左码右物”方法,则NaOH质量为2g-0.4g=1.6g,称量NaOH的质量偏小,则n偏小,浓度偏小,故D不选;
故选B.
点评 本题考查配制一定浓度的溶液,为高频考点,把握溶液配制的实验操作、浓度公式、误差分析为解答的关键,侧重分析与实验能力的考查,注意结合浓度公式分析误差,题目难度不大.

练习册系列答案
相关题目
4.下列试剂储存说法不正确的是( )
| A. | 金属钠存放在盛有煤油的试剂瓶中 | |
| B. | 烧碱盛放在玻璃瓶塞的磨口玻璃瓶中 | |
| C. | 氢氟酸不能保存在玻璃瓶内 | |
| D. | 漂白粉置于冷暗处密封保存 |
5.下列物质可作为食品防腐剂的是( )
| A. | 甲醛 | B. | 硼酸 | C. | 苯甲酸钠 | D. | 醋酸 |
2.锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述不正确的是( )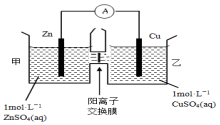

| A. | 铜电极上发生还原反应 | |
| B. | 电池工作一段时间后,甲池的c(SO42-)不变 | |
| C. | 电池工作一段时间后,乙池溶液的总质量增加 | |
| D. | 阴阳离子离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡 |
9.自然界中含量最多的金属元素和非金属元素形成的稳定化合物是( )
| A. | Al2O3 | B. | SiO2 | C. | Fe2O2 | D. | CaO |
2.下列有关焰色反应的叙述正确的是( )
| A. | 只有金属的化合物灼烧时才会有不同的颜色 | |
| B. | 每次实验后,铂丝都要用水洗净 | |
| C. | 若透过蓝色钴玻璃只看到紫色,说明样品中含钾元素而一定不含钠元素 | |
| D. | 若样品灼烧呈黄色,判断一定有钠元素,但不能排除含其他金属元素 |
9.能正确表示下列反应的离子方程式是( )
| A. | 向Fe(NO3)2稀溶液中加入盐酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O | |
| B. | 铝和氢氧化钠水溶液反应:Al+2OH-+2H2O═AlO2-+3H2↑ | |
| C. | 碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH4++OH- $\frac{\underline{\;△\;}}{\;}$NH3↑+H2O | |
| D. | AlCl3溶液中滴加足量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
7.将11.2g铁粉加到250mL 2mol/L的氯化铁溶液中,完全反应后,其结果是( )
| A. | 铁有剩余,溶液呈浅绿色,c(Cl-)基本不变 | |
| B. | 往溶液中滴加无色KSCN溶液,不显色 | |
| C. | 溶液中n(Fe2+)与n(Fe3+)之比为6:1 | |
| D. | 氧化产物与还原产物的物质的量之比为2:5 |
 ;
;