题目内容
下列离子方程式正确的是
A.FeSO4酸性溶液暴露在空气中: 4Fe2++O2+4H+ 4Fe3++2H2O
4Fe3++2H2O
B.过量石灰水与碳酸氢钙反应:Ca2++2HCO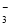 +2OH-===CaCO3↓+CO
+2OH-===CaCO3↓+CO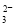 +2H2O
+2H2O
C.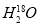 中投入Na2O2固体:2
中投入Na2O2固体:2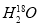 +2Na2O2===4OH-+4Na++18O2↑
+2Na2O2===4OH-+4Na++18O2↑
D.向氯化铝溶液中滴加过量氨水:Al3++4NH3·H2O===AlO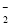 +4NH
+4NH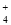 +2H2O
+2H2O
A
【解析】
试题分析:A、FeSO4酸性溶液暴露在空气中,Fe2+在H+条件下被O2氧化为Fe3+,离子方程式正确;B、过量石灰水与碳酸氢钙反应的离子方程式为:Ca2++OH?+HCO3?=CaCO3↓+H2O,错误;C、O2中的O元素来源于Na2O2,不是18O,错误;D、向氯化铝溶液中滴加过量氨水,生成Al(OH)3沉淀,错误。
考点:本题考查离子方程式的书写。

 阅读快车系列答案
阅读快车系列答案甲、乙、丙是三种不含相同离子的可溶性强电解质。它们所含离子如下表所示,取等质量的三种化合物配制相同体积的溶液,其溶质物质的量浓度:c(甲)>c(乙)>c(丙),则乙物质可能是
阴离子 | OH-、NO | 阳离子 | NH |
①MgSO4 ②NaOH ③(NH4)2SO4 ④Mg(NO3)2 ⑤NH4NO3
A.①② B.③④ C.③⑤ D.①⑤
相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g) 2NH3(g) △H=一92.6kJ/mol。实验测得起始、平衡时的有关数据如下表:
2NH3(g) △H=一92.6kJ/mol。实验测得起始、平衡时的有关数据如下表:
容器
| 起始各物质的物质的量/mol | 达平衡时体系能量的变化 | ||
N2 | H2 | NH3 | ||
① | 1 | 3 | 0 | 放出热量:23.15kJ |
② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
下列叙述不正确的是
A.容器①、②中反应的平衡常数相等
B.平衡时,两个容器中NH3的体积分数均为1/7
C.容器②中达平衡时放出的热量Q=23.15kJ
D.若容器①体积为0.5L,则平衡时放出的热量小于23.15kJ
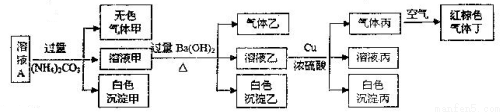
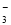 、SO
、SO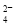
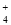 、Na+、Mg2+
、Na+、Mg2+