题目内容
甲、乙、丙是三种不含相同离子的可溶性强电解质。它们所含离子如下表所示,取等质量的三种化合物配制相同体积的溶液,其溶质物质的量浓度:c(甲)>c(乙)>c(丙),则乙物质可能是
阴离子 | OH-、NO | 阳离子 | NH |
①MgSO4 ②NaOH ③(NH4)2SO4 ④Mg(NO3)2 ⑤NH4NO3
A.①② B.③④ C.③⑤ D.①⑤
C
【解析】
试题分析:甲、乙、丙均是可溶性强电解质,则OH-只能与Na+组成NaOH,三种化合物不含相同离子,所以甲、乙、丙化合物有两种组合,第一组:NaOH、(NH4)2SO4、Mg(NO3)2;第二组:NaOH、NH4NO3、MgSO4,根据溶质质量相等,溶液体积相等以及物质的量浓度大小判断,相对分子质量:Mr(丙)>Mr(乙)>Mr(甲)。第一组:NaOH相对分子质量为40,(NH4)2SO4相对分子质量为132、Mg(NO3)2相对分子质量为148;第二组:NaOH相对分子质量为40、NH4NO3相对分子质量为80、MgSO4相对分子质量为120,所以乙可能是硫酸铵或硝酸铵,故C项正确。
考点:本题考查离子共存、物质的量浓度的计算。

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
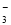 、SO
、SO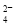
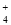 、Na+、Mg2+
、Na+、Mg2+
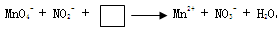 。下列叙述中正确的是
。下列叙述中正确的是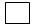 中的粒子是OH-
中的粒子是OH- 4Fe3++2H2O
4Fe3++2H2O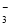 +2OH-===CaCO3↓+CO
+2OH-===CaCO3↓+CO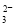 +2H2O
+2H2O 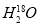 中投入Na2O2固体:2
中投入Na2O2固体:2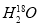 +2Na2O2===4OH-+4Na++18O2↑
+2Na2O2===4OH-+4Na++18O2↑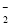 +4NH
+4NH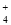 +2H2O
+2H2O