题目内容
(16分) A是有机羧酸盐HCOONa,B、C、D是常见化合物;A、B、C、D焰色反应呈黄色,水溶液均呈碱性,其中B的碱性最强。X、Y是最常见的氧化物且与人体、生命息息相关,它们的晶体类型相同。C受热分解得到Y、D和X;B与C反应生成D和X。E由两种元素组成,相对分子质量为83,将E投入X中得到B和气体Z,Z在标准状况下的密度为0.76g·L-1。
(1)E晶体中含有的化学键是 。Y的电子式是 。
(2)X的沸点比同主族同类型物质要高,原因是 。
(3)写出E与X反应的化学方程式 。
(4)写出在D的饱和溶液中不断通Y析出C的离子方程式 。
B与C反应生成D和X的离子方程式
(5)A的一个重要应用是根据2A→P+H2↑得到P,P溶液中的阴离子通常用CaC12使之沉淀,P的化学式 ,此反应是不是氧化还原反应
(16分)
(1)离子键(2分) 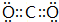 (2分)
(2分)
(2)水分子间存在氢键(2分)
(3)Na3N+3H2O==3NaOH+NH3(2分)
(4)2Na++CO32-+H2O+CO2====2NaHCO3↓(2分)
HCO3- + OH- == CO32-+H2O (2分)
(5)P的化学式Na2C2O4 , 是 (4分)
【解析】
试题分析:A是有机羧酸盐HCOONa,B、C、D是常见化合物; A、B、C、D焰色反应呈黄色,水溶液均呈碱性,则可推知化合物A、B、C、D均为含有Na元素的碱或强碱弱酸盐,B的碱性最强,则B为NaOH;X、Y是最常见的氧化物且与人体、生命息息相关,它们的晶体类型相同,则X、Y应为H2O和CO2中的一种,由C受热分解得到Y、D和X;B与C反应生成D和X,可推知C为NaHCO3,D为Na2CO3,即2NaHCO3 Na2CO3+CO2↑+H2O; NaHCO3+NaOH=Na2CO3+H2O,故X为H2O,Y为CO2.E由两种元素组成,式量为83,将E投入H2O中得到NaOH和气体Z,Z在标准状况下的密度为0.76g?L-1,可知气体Z的相对分子质量=0.76×22.4=17,则Z为NH3,由该反应:E+H2O→NaOH+NH3↑,可推知E由Na和N两种元素组成,可确定E是Na3N。
Na2CO3+CO2↑+H2O; NaHCO3+NaOH=Na2CO3+H2O,故X为H2O,Y为CO2.E由两种元素组成,式量为83,将E投入H2O中得到NaOH和气体Z,Z在标准状况下的密度为0.76g?L-1,可知气体Z的相对分子质量=0.76×22.4=17,则Z为NH3,由该反应:E+H2O→NaOH+NH3↑,可推知E由Na和N两种元素组成,可确定E是Na3N。
(1)上述分析可知E为Na3N,含有离子键,Y为CO2,电子式为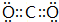 。
。
(2)X为H2O,水分子之间存在氢键,沸点高于同主族同类型物质。
(3)E与X反应的化学方程式为:Na3N+3H2O=3NaOH+NH3↑。
(4)D为Na2CO3,其饱和溶液中不断通入CO2,析出C为NaHCO3,反应的离子方程式为:2Na++CO32-+H2O+CO2=2NaHCO3↓;B与C反应生成D和是碳酸氢钠与氢氧化钠反应生成碳酸钠与水,离子方程式为:HCO3-+OH-=CO32-+H2O。
(5)反应2HCOONa→P+H2↑得到P,P溶液中的阴离子通常用CaC12使之沉淀,由守恒可知P为Na2C2O4,反应中有单质氢气生成,属于氧化还原反应。
考点:本题考查无机物推断、电子式及方程式的书写、氧化还原反应。

 春雨教育同步作文系列答案
春雨教育同步作文系列答案 。下列有关物质的推断不正确的是
。下列有关物质的推断不正确的是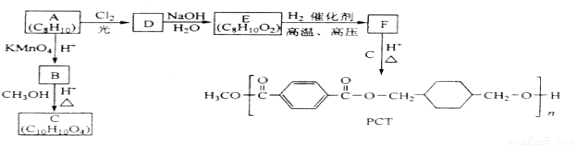
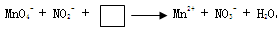 。下列叙述中正确的是
。下列叙述中正确的是 中的粒子是OH-
中的粒子是OH- 4Fe3++2H2O
4Fe3++2H2O +2OH-===CaCO3↓+CO
+2OH-===CaCO3↓+CO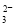 +2H2O
+2H2O 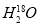 中投入Na2O2固体:2
中投入Na2O2固体:2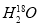 +2Na2O2===4OH-+4Na++18O2↑
+2Na2O2===4OH-+4Na++18O2↑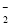 +4NH
+4NH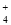 +2H2O
+2H2O