题目内容
1.几种短周期元素的原子半径及主要化合价见下表:| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A. | L、R 的单质与稀盐酸反应速率 L<R | |
| B. | L 与 T 形成的化合物具有两性 | |
| C. | Q、T 两元素的氢化物热稳定性 Q<T | |
| D. | L、Q 形成的简单离子核外电子数相等 |
分析 L和R的化合价都为+2价,应为周期表第ⅡA族,根据半径关系可知R为Be,L为Mg;Q和T的化合价都有-2价,应为周期表第ⅥA族元素,Q的最高价为+6价,应为S元素;T无正价,应为O元素;M的化合价为+3价,应为周期表第ⅢA族元素,根据M原子半径大于Q小于L可知应和L同周期,为Al元素,结合元素周期律知识解答该题.
解答 解:L和R的化合价都为+2价,应为周期表第ⅡA族,根据半径关系可知R为Be,L为Mg;Q和T的化合价都有-2价,应为周期表第ⅥA族元素,Q的最高价为+6价,应为S元素,T无正价,应为O元素;M的化合价为+3价,应为周期表第ⅢA族元素,根据M原子半径大于Q小于L可知应和L同周期,为Al元素,
A.金属性Mg>Al,则Mg与酸反应越剧烈,则相同条件下单质与稀盐酸反应速率为L>M,故A错误;
B.L为Mg、T为O,二者形成的化合物额MgO,氧化镁只能与酸反应,不能与碱溶液反应,所以氧化镁不具有两性,故B错误;
C.Q为S、T为O与酸,非金属性O>S,则对应氢化物的稳定性:Q<T,故C正确;
D.Mg2+核外有10个电子,S2-核外有18个电子,二者核外电子数不同,故D错误;
故选C.
点评 本题考查原子结构与元素周期律的关系,题目难度中等,正确把握元素化合价、原子半径与元素性质的关系是解答该题的关键,注意元素周期律的递变规律的应用.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
11.一定温度下,固定容器的密闭容器中进行的可逆反应:A(g)+B(g)?C(g)+D(g),当下列物理量不再改变时,表明反应已达到平衡的是( )
| A. | 单位时间内有1mol A生成,有1molC消耗 | |
| B. | 混合气体的密度不变 | |
| C. | A的消耗速率与D的消耗速率相同 | |
| D. | 混合物的平均相对分子质量不变 |
12.下列说法正确的是( )
| A. | 糖类化合物都具有相同的官能团 | |
| B. | 糖类是提供能量最高的营养物质 | |
| C. | 蛋白质的水解产物都含有羧基和氨基 | |
| D. | 酯类在碱性条件下的水解反应称为皂化反应 |
9.“绿色化学”是21世纪化学发展的主要方向.“绿色化学”要求从根本上消除污染,它包括“原料的绿色化”、“化学反应的绿色化”、“产物的绿色化”等内容.其中“化学反应的绿色化”要求反应物中所有的原子完全被利用且全部转入期望的产品中.下列符合“化学反应的绿色化”的是( )
| A. | SO2+2NH3+H2O═(NH4)2SO3 | |
| B. | NO2+NO+2NaOH═2NaNO2+H2O | |
| C. | Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O | |
| D. | CuO+H2SO4(稀)═CuSO4+H2O |
16.化学与生产、生活和社会密切相关.下列说法正确的是( )
| A. | 二氧化硫、氮氧化物和可入肺颗粒物是雾霾的主要成分,PM2.5 就是指大气中直径小于或等于 2.5 微米的可入肺颗粒物,雾霾都有丁达尔效应 | |
| B. | 屠呦呦最早提出用乙醚提取青蒿素,其提取物抗疟作用达 95%到 100%,这种提取原理就是萃取,属于物理过程 | |
| C. | 硅是一种良好的半导体材料,是制造光导纤维的基本原料 | |
| D. | 工业生产中,常在元素周期表金属与非金属分界线附近寻找催化剂 |
6.一定温度下在密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )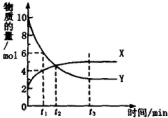

| A. | 反应的化学方程式为5Y?X | |
| B. | t1时,Y的浓度是X浓度的1.5倍 | |
| C. | t2时,正、逆反应速率相等,达到化学平衡 | |
| D. | t3时,逆反应速率大于正反应速率 |
13.下列各组物质的晶体中,所含化学键类型全部相同,熔化时所克服的作用力也完全相同是( )
| A. | CO2和 SiO2 | B. | NaCl 和 HCl | ||
| C. | (NH4)2CO3和 CO(NH2)2(尿素) | D. | NaH 和 KCl |