题目内容
(1)某有机物A的质量为9.2克,完全燃烧后生成0.4mol二氧化碳和10.8克水,且此有机物的蒸气的相对密度是相同状况下氢气的23倍,求:
①此有机物的分子式为
②写出该有机物可能的结构简式
(2)某烃B的相对分子质量为84.回答下列问题:
①下列物质与B以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不相等的是(填序号) .
a.C7H12O2 b.C6H14c.C6H14O d.C7H14O3
②若链烃B分子中所有的碳原子共平面,该分子的一氯取代物只有一种,则B的结构简式为 .
③若烃B不能使溴水褪色,并且其一氯代物只有一种,则B的结构简式为 .
(3)C1(一碳化学)是以含一个碳原子的化合物如:甲烷(CH4)、合成气(CO和H2)、CO2、CH3OH、HCHO等为初始反应物,反应合成一系列重要的化工原料和燃料的化学.
①CO与H2按一定比例可合成乙二醇(C2H6O2),则
= .
②汽油平均组成用CmHn表示,则合成汽油应控制
= .(用m、n表示)
①此有机物的分子式为
②写出该有机物可能的结构简式
(2)某烃B的相对分子质量为84.回答下列问题:
①下列物质与B以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不相等的是(填序号)
a.C7H12O2 b.C6H14c.C6H14O d.C7H14O3
②若链烃B分子中所有的碳原子共平面,该分子的一氯取代物只有一种,则B的结构简式为
③若烃B不能使溴水褪色,并且其一氯代物只有一种,则B的结构简式为
(3)C1(一碳化学)是以含一个碳原子的化合物如:甲烷(CH4)、合成气(CO和H2)、CO2、CH3OH、HCHO等为初始反应物,反应合成一系列重要的化工原料和燃料的化学.
①CO与H2按一定比例可合成乙二醇(C2H6O2),则
| n(CO) |
| n(H2) |
②汽油平均组成用CmHn表示,则合成汽油应控制
| n(CO) |
| n(H2) |
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:(1)根据该化合物的蒸气对氢气的相对密度可求得9.2克有机物的物质的量,根据CO2和H2O的质量判断9.2克有机物中是否含有O元素,并计算O原子的质量,进而计算C、H、O的物质的量比值,结合相对分子质量可得该有机物的化学式,并书写结构简式;
(2)①将各物质组成通式写成CxHyOz,各物质的(x+
-
)的值相等,则符合题意;
②烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种,则结构对称,只含一种H;
③不能使溴水褪色,且其一氯代物只有一种,则不含C=C,只有一种H,应为环烃;
(3)根据C、H元素守恒来计算物质的量.
(2)①将各物质组成通式写成CxHyOz,各物质的(x+
| y |
| 4 |
| z |
| 2 |
②烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种,则结构对称,只含一种H;
③不能使溴水褪色,且其一氯代物只有一种,则不含C=C,只有一种H,应为环烃;
(3)根据C、H元素守恒来计算物质的量.
解答:
解:(1)①n(CO2)=0.4mol,
则2.3g有机物中:n(C)=n(CO2)=0.4mol,m(C)=0.4mol×12g/mol=4.8g,
n(H2O)=
=0.6mol,
则9.2g有机物中:n(H)=2n(H2O)=1.2mol,m(H)=1.2mol×1g/mol=1.2g,
因(1.2g+4.8g)<9.2gg,
所以有机物中还应还用O元素,且m(O)=9.2g-4.8g-1.2g=3.2g,n(O)=
=0.2mol,
则有机物中:n(C):n(H):n(O)=0.4mol:1.2mol:0.2mol=2:6:1,
所以该有机物的最简式为C2H6O,又该化合物的蒸气对氢气的相对密度是23,则M=2×23=46,
而C2H6O的相对分子质量为46,所以,该有机物的分子式为C2H6O,
故答案为:C2H6O;
②分子式为C2H6O的有机物可以为乙醇或二甲醚,结构简式为:CH3CH2OH或CH3OCH3,故答案为:C2H5OH或CH3OCH3;
(2)①烃A的相对分子质量为84,则该烃可能为烯烃或环烷烃,分子式应为C6H12,
(1)总物质的量一定,充分燃烧消耗氧气的量不相等,则1molC6H12消耗氧气为x+
=9mol,
a.1molC7H12O2消耗氧气为9mol,总物质的量一定,充分燃烧消耗氧气的量相等,故a不选;
b.1molC6H14消耗氧气为9.5mol,总物质的量一定,充分燃烧消耗氧气的量不相等,故b选;
c.1molC6H14O消耗氧气为9mol,总物质的量一定,充分燃烧消耗氧气的量相等,故c不选;
d.1molC7H14O3消耗氧气为9mol,总物质的量一定,充分燃烧消耗氧气的量相等,故d不选;
故答案为:b;
(2)①烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种,则结构对称,只含一种H,即含4个甲基,A为 ,
,
故答案为: (或CH3)2C=C(CH3)2);
(或CH3)2C=C(CH3)2);
③烃B不能使溴水褪色,且其一氯代物只有一种,则不含C=C,只有一种H,应为环烃,其结构简式为 ,故答案为:
,故答案为: ;
;
(3)①CO与H2按一定比例可合成乙二醇(C2H6O2),根据碳元素和氢元素守恒,则
=
,故答案为:
;
②汽油平均组成用CmHn表示,根据碳元素和氢元素守恒,则合成汽油应控制
=
=
,故答案为:
.
则2.3g有机物中:n(C)=n(CO2)=0.4mol,m(C)=0.4mol×12g/mol=4.8g,
n(H2O)=
| 10.8g |
| 18g/mol |
则9.2g有机物中:n(H)=2n(H2O)=1.2mol,m(H)=1.2mol×1g/mol=1.2g,
因(1.2g+4.8g)<9.2gg,
所以有机物中还应还用O元素,且m(O)=9.2g-4.8g-1.2g=3.2g,n(O)=
| 3.2g |
| 16g/mol |
则有机物中:n(C):n(H):n(O)=0.4mol:1.2mol:0.2mol=2:6:1,
所以该有机物的最简式为C2H6O,又该化合物的蒸气对氢气的相对密度是23,则M=2×23=46,
而C2H6O的相对分子质量为46,所以,该有机物的分子式为C2H6O,
故答案为:C2H6O;
②分子式为C2H6O的有机物可以为乙醇或二甲醚,结构简式为:CH3CH2OH或CH3OCH3,故答案为:C2H5OH或CH3OCH3;
(2)①烃A的相对分子质量为84,则该烃可能为烯烃或环烷烃,分子式应为C6H12,
(1)总物质的量一定,充分燃烧消耗氧气的量不相等,则1molC6H12消耗氧气为x+
| y |
| 4 |
a.1molC7H12O2消耗氧气为9mol,总物质的量一定,充分燃烧消耗氧气的量相等,故a不选;
b.1molC6H14消耗氧气为9.5mol,总物质的量一定,充分燃烧消耗氧气的量不相等,故b选;
c.1molC6H14O消耗氧气为9mol,总物质的量一定,充分燃烧消耗氧气的量相等,故c不选;
d.1molC7H14O3消耗氧气为9mol,总物质的量一定,充分燃烧消耗氧气的量相等,故d不选;
故答案为:b;
(2)①烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种,则结构对称,只含一种H,即含4个甲基,A为
 ,
,故答案为:
 (或CH3)2C=C(CH3)2);
(或CH3)2C=C(CH3)2);③烃B不能使溴水褪色,且其一氯代物只有一种,则不含C=C,只有一种H,应为环烃,其结构简式为
 ,故答案为:
,故答案为: ;
;(3)①CO与H2按一定比例可合成乙二醇(C2H6O2),根据碳元素和氢元素守恒,则
| n(CO) |
| n(H2) |
| 2 |
| 3 |
| 2 |
| 3 |
②汽油平均组成用CmHn表示,根据碳元素和氢元素守恒,则合成汽油应控制
| n(CO) |
| n(H2) |
| m | ||
m+
|
| 2m |
| 2m+n |
| 2m |
| 2m+n |
点评:本题是一道关于有机物的结构和性质的综合知识的考查题,注意知识的归纳和整理是关键,难度不大.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
下列离子方程式正确的是( )
| A、碳酸氢钠溶液中滴入少量氢氧化钙溶液:HCO3-+OH-=CO32-+H2O |
| B、硅酸钠溶液与醋酸溶液混合:SiO32-+2H+=H2SiO3↓ |
| C、0.01mol/L NH4Al(SO4)2溶液与0.02mol/L Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3?H2O |
| D、向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
下列检验试剂选用正确的是( )
| A、用氯水、KSCN溶液检验FeCl3中是否有FeCl2溶液 |
| B、用酸性KMnO4溶液检验FeCl3中是否有FeCl2 |
| C、用NaOH溶液检验MgCl2中是否有FeCl2 |
| D、用硝酸检验某黄色固体是纯铜还是黄铜 |
下列表示对应化学反应的离子方程式正确的是( )
| A、向NaAlO2溶液中通入过量CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- |
| B、Cl2与水的反应:Cl2+H2O═2H++Cl-+ClO- |
| C、醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
| D、FeCl3溶液与Cu的反应:Cu+Fe3+═Cu2++Fe2+ |
 A、B、C、D为原子序数依次增大的前四周期元素,元素A原子最外层电子数比内层多3个,元素B基态原子核外有2个未成对电子,元素C的最高价和最低价代数和等于0,元素D位于周期表ⅥB族.
A、B、C、D为原子序数依次增大的前四周期元素,元素A原子最外层电子数比内层多3个,元素B基态原子核外有2个未成对电子,元素C的最高价和最低价代数和等于0,元素D位于周期表ⅥB族.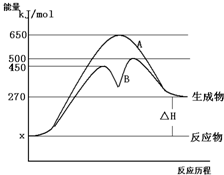 反应物与生成物均为气态的某可逆反应在不同条件下的反应历程分别为A、B,如图所示.
反应物与生成物均为气态的某可逆反应在不同条件下的反应历程分别为A、B,如图所示.