题目内容
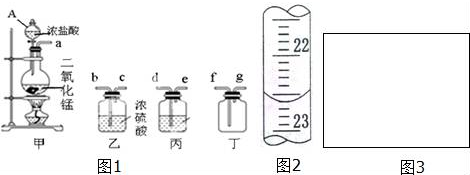
18.根据实验室制取某干燥气体的装置图(如图所示),判断气体发生装置中的药品可能是( )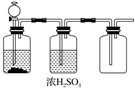
| A. | FeS和稀H2SO4 | B. | 加热NaCl和浓H2SO4制HCl | ||
| C. | 大理石和稀盐酸 | D. | MnO2和浓盐酸 |
分析 由装置图可知,在常温下反应生成的气体可用浓硫酸干燥,且用向上排空法收集气体,说明气体的密度比空气大,以此解答该题.
解答 解:A.FeS和稀H2SO4反应生成硫化氢气体,具有还原性,不能用浓硫酸干燥,故A错误;
B.装置不能加热,则不能用于制备氯化氢,故B错误;
C.大理石和稀盐酸生成二氧化碳,可用浓硫酸干燥,且二氧化碳密度比空气大,可用向上排空法收集,故C正确;
D.二氧化锰和浓盐酸需要加热条件下制备氯气,而本题装置不能加热,故D错误.
故选C.
点评 本题考查常见气体的干燥和收集,为高频考点,侧重于学生的分析、实验能力的考查,做题时要充分考虑物质的性质,认真分析实验装置图的特点,从而做出正确判断.

练习册系列答案
相关题目
8. 如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni电池).下列有关说法不正确的是( )
如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni电池).下列有关说法不正确的是( )
 如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni电池).下列有关说法不正确的是( )
如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni电池).下列有关说法不正确的是( )| A. | 放电时正极反应为:NiOOH+H2O+e-=Ni(OH)2+OH- | |
| B. | 电池的电解液可为KOH溶液 | |
| C. | 充电时负极反应为:MH+OH-=M+H2O+e- | |
| D. | MH是一类储氢材料,其氢密度越大,电池的能量密度越高 |
3.能正确表示下列反应的离子方程式是( )
| A. | Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-=2Fe2++I2+3H2O | |
| B. | 0.1mol/LNH4Al(SO4)2溶液与0.2mol/LBa(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-=2BaSO4+AlO2-+2H2O | |
| C. | 向NaHCO3溶液中滴加盐酸:CO32-+2H+=H2O+CO2↑ | |
| D. | 向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O=HClO+HSO3- |
10.能正确表示下列反应的离子方程式是( )
| A. | 醋酸钠的水解反应:CH3COO-+H2O═CH3COOH+OH- | |
| B. | 碳酸氢钙与过量的NaOH溶液反应Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32- | |
| C. | 苯酚钠溶液与过量二氧化碳反应:C6H5O-+CO2+H2O═C6H5OH+CO32- | |
| D. | 稀硝酸与过量的铁屑反应:3Fe+8H++2NO3-═3 Fe3++2NO↑+4H2O |
7.纳米材料的表面粒子数占粒子总数的比例很大,这是它有许多特殊性质的原因.假设某硼镁化合物的结构如图所示(六个硼原子位于棱柱内),则这种纳米颗粒的表面粒子数占总粒子数的百分比为( )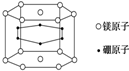

| A. | 22% | B. | 70% | C. | 66.7% | D. | 33.3% |