题目内容
2.明代宋应星著的《天工开物》中有关于“火法”冶炼锌的工艺记载:“炉甘石十斤,装载入一泥罐内,…然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,…,冷淀,毁罐取出,…,即倭铅也.”下列说法不正确的是(注:炉甘石的主要成分为碳酸锌)( )| A. | 该冶炼锌的反应属于置换反应 | |
| B. | 煤炭中起作用的主要成分是C | |
| C. | 冶炼Zn的反应方程式为:ZnCO3+2C$\frac{\underline{\;高温\;}}{\;}$Zn+3CO↑ | |
| D. | 倭铅是指金属锌和铅的混合物 |
分析 碳酸锌与碳在高温下反应生成锌和一氧化碳,反应的方程式为ZnCO3+2C$\frac{\underline{\;高温\;}}{\;}$Zn+3CO↑,据此分析.
解答 解:碳酸锌与碳在高温下反应生成锌和一氧化碳,反应的方程式为ZnCO3+2C$\frac{\underline{\;高温\;}}{\;}$Zn+3CO↑,
A.该冶炼锌的反应属于置换反应,故A正确;
B.反应中C作还原剂,则煤炭中起作用的主要成分是C,故B正确;
C.冶炼Zn的反应方程式为:ZnCO3+2C$\frac{\underline{\;高温\;}}{\;}$Zn+3CO↑,故C正确;
D.由题意可知,倭铅是指金属锌,故D错误.
故选D.
点评 本题以锌的冶炼为知识背景,考查了置换反应、方程式的书写、题目信息的应用等,题目难度中等,侧重于考查学生的阅读能力和对信息的应用能力.

练习册系列答案
相关题目
13.如图是可逆反应A+2B?2C+3D的反应速率随反应时间变化的示意图,由此可推断( )
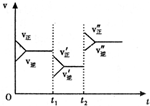

| A. | t1时若是降温使速率变化,则正确反应是放热反应 | |
| B. | t2时若是加压使速度变化,则A、B、C、D均为气体 | |
| C. | t2时改变的条件可能是加入催化剂 | |
| D. | t2时改变的条件可能是增大反应物的浓度 |
10.常温下,下列溶液中各离子浓度关系正确的是( )
| A. | 浓度为0.1 mol•L-1的碳酸钠溶液:c(Na+)=2c(CO32-)+c(HCO3-)+c(H2CO3) | |
| B. | pH=12的氨水溶液与pH=2的盐酸等体积混合:c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| C. | 等物质的量的氨水和盐酸混合后的溶液:c(H+)=c(OH-)+c(NH3•H2O) | |
| D. | 醋酸溶液与NaOH溶液相混合后,所得溶液呈中性:c(Na+)>c(CH3COO-) |
17.化学与生活密切相联,下列应用中利用了物质的氧化性的是( )
| A. | SO2漂白纸浆 | B. | 纯碱清洗油污 | ||
| C. | Na2S除污水中的Cu2+ | D. | 漂白粉漂白织物 |
7.某同学将光亮的镁条放入盛有NH4Cl溶液的试管中,有大量气泡产生.为探究其反应原理,该同学做了以下实验并观察到相关现象,由此得出的结论不合理的是( )
| 选项 | 实验及现象 | 结论 |
| A | 将湿润的红色石蕊试纸放在试管口,试纸变蓝 | 反应中有NH3产生 |
| B | 收集产生的气体并点燃,火焰呈淡蓝色 | 反应中有H2产生 |
| C | 收集气体的同时测得溶液的pH为8.6 | 溶液中OH?氧化了Mg |
| D | 将光亮的镁条放入pH为8.6的NaHCO3溶液中,有气泡产生 | 弱碱性溶液中Mg也可被氧化 |
| A. | A | B. | B | C. | C | D. | D |
14.室温下,1mol•L-1的二元酸H2A溶液体系中存在的所有含A粒子(HA-、A2-)所占的物质的量分数(δ)随pH变化的关系如图所示,下列说法不正确的是( )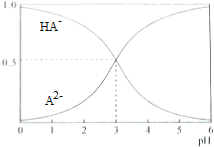

| A. | pH=5时,c(HA-)>c(A2-)>c(H+)>c(OH-) | |
| B. | 在Na2A溶液中存在c(Na+)=2c(A2-)+2c(HA-) | |
| C. | 等物质的量浓度的NaHA和Na2A混合溶液中,c(Na+)>c(A2-)>c(HA-) | |
| D. | 电离平衡HA-?A2-+H+的平衡常数Ka=10-3 |
11.已知酸性溶液中还原性的顺序为SO32->I->Fe2+>Br->Cl-,下列反应不能发生的是( )
| A. | 2Fe3++SO32-+H2O→2Fe2++SO42-+2H+ | |
| B. | I2+SO32-+H2O→SO42-+2I-+2H+ | |
| C. | 2Fe2++I2→2Fe3++2I- | |
| D. | Br2+SO32-+H2O→SO42-+2Br-+2H+ |
4.某学习小组进行了如下课外活动,邀请你参与:
(1)研究水溶液中复分解型离子反应的发生条件,设计如下方案:
①写出II实验中发生反应的离子方式:H++CH3COO-=CH3COOH.
②根据实验发现只要有气体、沉淀、弱电解质等物质生成,水溶液中复分解型离子反应就可以发生.
③经过小组同学积极思考、讨论交流发现在生成三类物质后,导致一个共同的结果,于是得出结论:溶液中复分解型的离子反应总是向着某些离子浓度减小 的方向进行(与溶液混合的瞬间相比).
④小组同学进一步深入思考,发现上述问题其实质是化学反应进行的方向问题.请你结合化学反应原理的相关知识对③中的结论作出合理解释:当生成上述三类物质时,形成新的化学键而导致体系的焓减或生成气体而导致熵增,由化学反应进行的方向的焓判据和熵判据知,反应可发生.
(2)如何研究H2SO4、KC1、NaHSO4、NaN03、Na2C03、NH4C1、NaOH的性质?设计方案为:将它们按照酸、碱、盐分类,然后分别溶于水得到溶液,进行实验,具体如下:
①根据方案进行分类时,经实验测得KC1、NaN03,溶液的pH=7;
H2SO4、NaHSO4、NH4Cl溶液的pH<7;
Na2C03、NaOH溶液的pH>7.
由此有的同学按分类法思想把H2SO4、NaHSO4、NH4Cl都划分为酸类,请你运用中学化学相关理论判断这样划分是否合理?并简要说明理由.不合理、硫酸氢钠和氯化铵都属于盐,前者电离产生的阳离子除了氢离子还有钠离子,后者是因为水解而显酸性.
②向NaHS04、NaN03的混合溶液中,滴加Na2S溶液产生黄色沉淀和无色气体,写出反应的离子方程式:2NO3-+3S2-+8H+=2NO↑+3S↓+4H2O.反应中若生成标准状况下的无色气体1.12L,则被氧化的物质为0.075mol,转移电子的物质的量为0.15mol.
③某同学在用H2S04鉴别NaN03、Na2C03、NaOH溶液时,Na2C03很容易鉴别,但鉴别NaN03和NaOH时却陷入了困境.限用上述另外六种物质,请你设计一个现象明显的实验方案帮忙解决这一难题:
(1)研究水溶液中复分解型离子反应的发生条件,设计如下方案:
| 实验设计及操作 | 离子方程式 |
| Ⅰ.向盛有2mlCuSO4溶液的试管里加入2mlNaOH溶液,观察现象 | Cu2++2OH-═Cu(OH)2↓ |
| Ⅱ.向盛有2mL pH=1的HCl溶液的试管里慢慢滴入18mL(已足量)CH3COONH4溶液(查资料知CH3COONH4,溶液呈中性 )震荡摇匀,测得pH≈3.7 | |
| Ⅲ向盛有2mLNaHCO3溶液的试管里加入2mL H2SO4溶液,观察现象 | HCO${\;}_{3}^{-}$+H+═H2O+CO2↑ |
| Ⅳ向盛有2mL 稀Na2SO4溶液的试管里加入2mL稀KCl溶液,观察无明显现象 |  |
②根据实验发现只要有气体、沉淀、弱电解质等物质生成,水溶液中复分解型离子反应就可以发生.
③经过小组同学积极思考、讨论交流发现在生成三类物质后,导致一个共同的结果,于是得出结论:溶液中复分解型的离子反应总是向着某些离子浓度减小 的方向进行(与溶液混合的瞬间相比).
④小组同学进一步深入思考,发现上述问题其实质是化学反应进行的方向问题.请你结合化学反应原理的相关知识对③中的结论作出合理解释:当生成上述三类物质时,形成新的化学键而导致体系的焓减或生成气体而导致熵增,由化学反应进行的方向的焓判据和熵判据知,反应可发生.
(2)如何研究H2SO4、KC1、NaHSO4、NaN03、Na2C03、NH4C1、NaOH的性质?设计方案为:将它们按照酸、碱、盐分类,然后分别溶于水得到溶液,进行实验,具体如下:
①根据方案进行分类时,经实验测得KC1、NaN03,溶液的pH=7;
H2SO4、NaHSO4、NH4Cl溶液的pH<7;
Na2C03、NaOH溶液的pH>7.
由此有的同学按分类法思想把H2SO4、NaHSO4、NH4Cl都划分为酸类,请你运用中学化学相关理论判断这样划分是否合理?并简要说明理由.不合理、硫酸氢钠和氯化铵都属于盐,前者电离产生的阳离子除了氢离子还有钠离子,后者是因为水解而显酸性.
②向NaHS04、NaN03的混合溶液中,滴加Na2S溶液产生黄色沉淀和无色气体,写出反应的离子方程式:2NO3-+3S2-+8H+=2NO↑+3S↓+4H2O.反应中若生成标准状况下的无色气体1.12L,则被氧化的物质为0.075mol,转移电子的物质的量为0.15mol.
③某同学在用H2S04鉴别NaN03、Na2C03、NaOH溶液时,Na2C03很容易鉴别,但鉴别NaN03和NaOH时却陷入了困境.限用上述另外六种物质,请你设计一个现象明显的实验方案帮忙解决这一难题: