题目内容
13.电子计算器所用的纽扣式电池为银锌电池,其电极分别为Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Ag2O+Zn+H2O═Zn(OH)2+2Ag,下列叙述中正确的是( )| A. | 电子由锌经导线流向Ag2O | |
| B. | 负极的电极反应为Zn-2e-═Zn2+ | |
| C. | 溶液中OH-向正极移动 | |
| D. | 随着电极反应的不断进行,电解质的碱性减弱 |
分析 该电池中Zn失电子为负极,负极电极反应式为Zn+2OH--2e-=Zn(OH)2;正极是Ag2O,正极的电极反应式为Ag2O+H2O+2e-=2Ag+2OH-,电子从负极经导线流向正极,内电路中阴离子移向负极,根据反应式确定溶液碱性变化.
解答 解:A.该电池中Zn失电子为负极,电子从负极经导线流向正极Ag2O,故A正确;
B.该电池中Zn失电子为负极,负极电极反应式为Zn+2OH--2e-=Zn(OH)2,故B错误;
C.电池工作时,阴离子氢氧根移向负极,故C错误;
D.电解质溶液为KOH溶液,电极反应为Ag2O+Zn+H2O═Zn(OH)2+2Ag,可知反应消耗水,溶液OH-浓度增大,则碱性增强,故D错误;
故选A.
点评 本题考查了原电池原理,侧重于学生的分析能力的考查,为高频考点,难度不大,注意把握原电池的工作原理和电极方程式的判断.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
3.能确定淀粉部分水解的试剂是( )
| A. | 碘液 | B. | 银氨溶液 | C. | 碘液和银氨溶液 | D. | 碘液或银氨溶液 |
4.运用元素周期律分析下列推断,其中错误的是( )
| A. | 铍的最高价氧化物的水化物可能具有两性 | |
| B. | 砹单质是有色固体,砹化氢很不稳定 | |
| C. | 碳酸锶难溶于水,但易溶于盐酸 | |
| D. | 砷的最高价氧化物的水化物是一种强酸 |
1.在一定条件下,动植物油脂与醇反应可制备生物柴油,化学方程式如下:
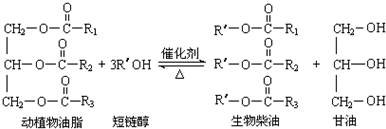
下列叙述正确的是( )

下列叙述正确的是( )
| A. | “地沟油”可用于制备生物柴油 | B. | 生物柴油属于油脂 | ||
| C. | 该反应属于酯化反应 | D. | 生物柴油的氧化反应是吸热反应 |
8.下列有关230Th和232Th的说法正确的是( )
| A. | 230Th和232Th的核外电子数不同 | B. | 230Th和232Th的化学性质不同 | ||
| C. | 230Th和232Th互为同位素 | D. | 230Th和232Th是同一种核素 |
18.已知:H2CO3 Ka1=4.3×10-7Ka2=5.61×10-11
HClO Ka=2.95×10-8 CaCO3 Ksp=2.8×10-9
下列离子方程式书写正确的是( )
HClO Ka=2.95×10-8 CaCO3 Ksp=2.8×10-9
下列离子方程式书写正确的是( )
| A. | 向碳酸氢镁溶液中加入足量的氢氧化钡溶液:Mg2++2HCO3-+2OH-═MgCO3↓+CO32-+2H2O | |
| B. | 向NaClO溶液通入少量CO2的离子反应方程式:2ClO-+CO2+H2O═2HClO+CO32- | |
| C. | 用惰性电极电解氯化镁溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH- | |
| D. | 向Ca(ClO)2溶液中通入少量CO2的离子反应方程式:Ca2++2ClO-+CO2+H2O═2HClO+CaCO3↓ |
5.下列说法正确的是( )
| A. | CH3CH2OH和CH3OCH3互为同分异构体 | |
| B. | 原子核内有8个中子的氧原子:${\;}_8^{18}O$ | |
| C. | CH3CH2CH2CH3的一氯代烃只有一种 | |
| D. |  为3-甲基-2-乙基丁烷 为3-甲基-2-乙基丁烷 |
2.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温常压下,8g CH4含有4NA个氢原子 | |
| B. | 1 mol Cu与足量FeCl3溶液反应,转移2NA个电子 | |
| C. | 1L 0.1 mol/L (NH4)2SO4溶液中含有0.2NA个NH4+ | |
| D. | 10 L pH=l 的硫酸溶液中含有的H+离子数为2NA |
3.下列叙述正确的是( )
| A. | 40 K和40 Ca原子中的质子数和中子数都相等 | |
| B. | 某元素最外层只有一个电子,则它一定是金属元素 | |
| C. | 任何原子或离子的组成中都含有质子 | |
| D. | 同位素的不同核素物理、化学性质完全相同 |