题目内容
在下列各说法中,正确的是( )
| A、△H>0表示放热反应,△H<0表示吸热反应 |
| B、热化学方程式中的化学计量数只表示物质的量,不能表示分子个数 |
| C、热化学方程式中的△H的值与各物质的状态、化学计量数、反应条件均有关 |
| D、1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、焓变△H>0表示吸热反应,△H<0,表示放热反应;
B、热化学方程式中的化学计量既表示物质的量也可以表示个数;
C、反应热与反应条件无关;
D.据燃烧热的概念分析.
B、热化学方程式中的化学计量既表示物质的量也可以表示个数;
C、反应热与反应条件无关;
D.据燃烧热的概念分析.
解答:
解:A.焓变△H>0表示吸热反应,△H<0,表示放热反应,故A错误;
B.热化学方程式中的化学计量既表示物质的量也可以表示个数,所以可以是分数,故B正确;
C.反应热的大小与反应条件无关,故C错误;
D.1mol氢气与氧气反应生成液态水时放出的热量才是氢气的燃烧热,故D错误.
故选B.
B.热化学方程式中的化学计量既表示物质的量也可以表示个数,所以可以是分数,故B正确;
C.反应热的大小与反应条件无关,故C错误;
D.1mol氢气与氧气反应生成液态水时放出的热量才是氢气的燃烧热,故D错误.
故选B.
点评:本题考查热化学方程式,燃烧热,注意燃烧热的概念,题目难度中等.

练习册系列答案
相关题目
在一定条件下,5molH2与1molN2在密闭容器中反应,达平衡时H2的转化率可能是( )
| A、100% | B、80% |
| C、60% | D、40% |
工业酒精中常含有甲醇,甲醇有剧毒,不能食用,其分子结构可能如图所示的模型表示.下列有关甲醇的叙述中,错误的是( )
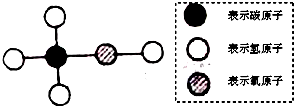

| A、甲醇的化学式为CH4O |
| B、甲醇的相对分子质量为32 |
| C、甲醇中C、H、O三种元素的质量比为1:4:1 |
| D、甲醇中氧元素的质量分数为50% |
各种洗涤剂广泛进入人们的生活中,下列洗涤中所用洗涤剂具有乳化功能的是( )
| A、用汽油除去衣服上的油污 |
| B、用餐具洗洁精清洗餐具上的油污 |
| C、用水洗去盘子中的水果渣 |
| D、用醋洗去水壶的水垢 |
现有两种高聚物A、B,已知A能溶于氯仿等有机溶剂,并加热到一定条件下熔融成粘稠的液体,B不溶于任何溶剂,加热不会变软或熔融,则下列叙述中一定不正确的是( )
| A、高聚物A可能具有弹性,B可能没有弹性 |
| B、高聚物A可能是线型高分子材料 |
| C、高聚物A一定是体型高分子材料 |
| D、高聚物B可能是体型高分子材料 |
根据下列反应,判断M、N、P的还原性由强到弱的顺序( )
①NCl2+P═N+PCI2
②2MCl3+3N═2M+3NCl2.
①NCl2+P═N+PCI2
②2MCl3+3N═2M+3NCl2.
| A、M>N>P |
| B、P>N>M |
| C、P>M>N |
| D、N>M>P |
下列除去杂质的方法错误的是( )
| A、用蒸馏的方法分离溴和CCl4的混合物 |
| B、除去Cl2中的少量HCl:通入NaOH溶液,收集气体 |
| C、除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤 |
| D、除去镁中的铝:加足量的NaOH溶液,过滤 |
 CrO2Cl2在有机合成中可作氧化剂或氯化剂,能与许多有机物反应,可用重铬酸钾与四氯化碳反应制备:
CrO2Cl2在有机合成中可作氧化剂或氯化剂,能与许多有机物反应,可用重铬酸钾与四氯化碳反应制备: