题目内容
下列装置或操作不能达到实验目的是( )
A、 制备氢氧化亚铁并观察其颜色 |
B、 用浓硫酸干燥Cl2 |
C、 检查装置的气密性 |
D、 利用排空气法收集CO2 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.制备氢氧化亚铁时应防止氧化;
B.洗气时注意气体的进出方向;
C.检验气密性时,根据形成压强差原理进行气密性的检查;
D.二氧化碳密度比空气大,可用向上排空法收集.
B.洗气时注意气体的进出方向;
C.检验气密性时,根据形成压强差原理进行气密性的检查;
D.二氧化碳密度比空气大,可用向上排空法收集.
解答:
解:A.氢氧化亚铁易被氧化,胶头滴管应插入到液面以下,故A错误;
B.洗气时,氯气从长导管进入溶液,故B正确;
C.检验气密性时,可先关闭止水夹,从长颈漏斗口加入水至形成液面差,如一段时间内液面不发生变化,在说明气密性良好,可用于检验气密性,故C正确;
D.二氧化碳密度比空气大,可用向上排空法收集,故D正确;故选A.
B.洗气时,氯气从长导管进入溶液,故B正确;
C.检验气密性时,可先关闭止水夹,从长颈漏斗口加入水至形成液面差,如一段时间内液面不发生变化,在说明气密性良好,可用于检验气密性,故C正确;
D.二氧化碳密度比空气大,可用向上排空法收集,故D正确;故选A.
点评:本题考查较为综合,涉及氢氧化亚铁的制备、气体的干燥、气密性的检查以及气体的收集等操作,侧重于学生的分析能力和实验能力的考查,为高考常见题型,注意把握物质的性质异同以及实验的严密性、可行性的评价,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
设阿伏加德罗常数为NA,下列叙述中正确的是( )
| A、常温常压下,32克氧气中原子个数为NA |
| B、标准状况下,1mol H2O的体积为22.4L |
| C、常温常压下,1mol H2的质量为2克 |
| D、物质的量浓度为0.5mol/L的MgCl2溶液中,含有的Cl-数为NA |
常温下,有关下列4种溶液的说法正确的是( )
| ① | ② | ③ | ④ |
| 0.1mol?L-1氨水 | Ph=11 氨水 |
0.1mol?L-1 盐酸 |
pH=3 盐酸 |
| A、由水电离出的c(H+):③>① |
| B、①稀释到原来的100倍,pH与②相同 |
| C、①与③混合,若溶液pH=7,则溶液中c(NH4+)>C(Cl-) |
| D、②与④等体积混合,混合液pH>7 |
废电池必须进行集中处理的主要原因是( )
| A、利用电池外壳的金属材料 |
| B、防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 |
| C、防止电池中渗泄的电解液腐蚀其他物品 |
| D、回收其中的石墨电极 |
下列说法正确的是( )
| A、常温下0.1 mol/L的下列溶液①NH4Al(SO4)2、②NH4Cl、③NH3?H2O、④CH3COONH4溶液中c(NH4+)由大到小的顺序是:②>①>④>③ |
| B、常温下0.4 mol/L HB溶液 和0.2 mol/L NaOH溶液等体积混合后溶液的pH=3,则溶液中离子浓度大小顺序为:c(HB)>c(Na+)>c(B-)>c(H+)>c(OH-) |
| C、pH=2的CH3COOH溶液和HCl溶液、pH=12的氨水和NaOH溶液,相同温度时,四种溶液中由水电离的c(H+)相等 |
| D、用惰性电极电解足量的CuSO4溶液一段时间,加入一定量的Cu(OH)2可以恢复至原来的浓度和体积 |
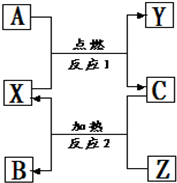 A、B、C是中学化学常见的单质,X、Y、Z是中学化学常见的氧化物,它们之间有如右图所示的转化关系,请据图回答:
A、B、C是中学化学常见的单质,X、Y、Z是中学化学常见的氧化物,它们之间有如右图所示的转化关系,请据图回答: 某研究性学习小组用0.20mol?L-1的标准NaOH溶液滴定未知浓度的盐酸,其实验探究操作为如下几步:
某研究性学习小组用0.20mol?L-1的标准NaOH溶液滴定未知浓度的盐酸,其实验探究操作为如下几步: 在①CO2、②NO2、③CO、④Cl2、⑤HCl、⑥NH3等气体中(选填序号)
在①CO2、②NO2、③CO、④Cl2、⑤HCl、⑥NH3等气体中(选填序号)