��Ŀ����
��1mol CO��1mol H2O��g������ij�̶��ݻ��ķ�Ӧ������ij�����´ﵽƽ�⣺CO��g��+H2O��g��?CO2��g��+H2��g������ʱ��
��COת��ΪCO2��
��1����ƽ��������CO2���������Ϊ ��
��2��������ͬ�����£��������г���1mol CO2��1mol H2��1mol H2O����ﵽƽ��ʱ�루1����Ƚϣ�ƽ��Ӧ�� �ƶ��������Ӧ�������淴Ӧ������������ʱƽ���ϵ�CO2������������������и�ֵ�е� �����ţ���
A.22.2% B.27.55% C.33.3% D.36.8%
��3�����磨2����ƽ��������Ӧ�����ƶ�ʱ��������˵������ȷ���� ������ţ�
��������IJ���һ������
����������������һ������
�۷�Ӧ���ת����һ������
�ܷ�Ӧ���Ũ��һ������
������Ӧ����һ�������淴Ӧ����
��һ��ʹ���˴�����
| 2 |
| 3 |
��1����ƽ��������CO2���������Ϊ
��2��������ͬ�����£��������г���1mol CO2��1mol H2��1mol H2O����ﵽƽ��ʱ�루1����Ƚϣ�ƽ��Ӧ��
A.22.2% B.27.55% C.33.3% D.36.8%
��3�����磨2����ƽ��������Ӧ�����ƶ�ʱ��������˵������ȷ����
��������IJ���һ������
����������������һ������
�۷�Ӧ���ת����һ������
�ܷ�Ӧ���Ũ��һ������
������Ӧ����һ�������淴Ӧ����
��һ��ʹ���˴�����
���㣺��ѧƽ��ļ���,��ѧƽ���Ӱ������
ר�⣺��ѧƽ��ר��
���������ݻ�ѧƽ������ʽ��ʽ���㣬
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ����mol�� 1 1 0 0
�仯����mol��
ƽ������mol��
��1���������=
��100%��
��2��������ͬ�����£��������г���1mol CO2��1mol H2��1mol H2O����ֵת���൱�ڼ���1molCO2��2molH2O����ﵽƽ��ʱ�루1����Ƚϣ����ڼ���1molˮƽ��������У�����ƽ��Ũ�ȼ���ƽ��Ũ�ȣ�����õ�ƽ�ⳣ��=
����ϻ�ѧƽ������ʽ��ʽ���㣻
��3��ƽ��������Ӧ�����ƶ������淴Ӧ������������Ӧ������������淴Ӧ���ʣ����������ʵ�������������Ӧǰ������������䣬�������壬�������������С�������ı䷴Ӧ���ʲ��ı仯ѧƽ�⣬��ϻ�ѧƽ���ƶ�ԭ���ͷ�Ӧ����ѡ�
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ����mol�� 1 1 0 0
�仯����mol��
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
ƽ������mol��
| 1 |
| 3 |
| 1 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
��1���������=
| ������̼���ʵ��� |
| ����������ʵ��� |
��2��������ͬ�����£��������г���1mol CO2��1mol H2��1mol H2O����ֵת���൱�ڼ���1molCO2��2molH2O����ﵽƽ��ʱ�루1����Ƚϣ����ڼ���1molˮƽ��������У�����ƽ��Ũ�ȼ���ƽ��Ũ�ȣ�����õ�ƽ�ⳣ��=
| ������ƽ��Ũ���ݴη��˻� |
| ��Ӧ��ƽ��Ũ���ݴη��˻� |
��3��ƽ��������Ӧ�����ƶ������淴Ӧ������������Ӧ������������淴Ӧ���ʣ����������ʵ�������������Ӧǰ������������䣬�������壬�������������С�������ı䷴Ӧ���ʲ��ı仯ѧƽ�⣬��ϻ�ѧƽ���ƶ�ԭ���ͷ�Ӧ����ѡ�
���
�⣺��������ʽ����ƽ��ʱ����ָ�Ũ�ȣ�
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ����mol�� 1 1 0 0
�仯����mol��
ƽ������mol��
��1����Ӧǰ�������������䣬����ƽ��ʱ�����������ܵ����ʵ���Ϊ1mol+1mol=2mol��
����ƽ��������CO2���������Ϊ=
��100%=33.3%��
�ʴ�Ϊ��33.3%��
��2������1mol CO2��lmol H2��1mol H2O����Ӧ���淴Ӧ���н���ƽ�⣬��ЧΪ��1����ƽ����ټ�1molH2O��g����ƽ��������Ӧ�ƶ���
��ѧƽ�ⳣ��=������ƽ��Ũ��ϵ���η�֮���뷴Ӧ��ƽ��Ũ��ϵ���η�֮���ıȣ�
�ʸ÷�Ӧ��ƽ�ⳣ������ʽk=
����Ӧ��ͬһ�����ڽ��У������ͬ������ʽ�и����ʵĻ�ѧ����������1�������ڼ����о��������ʵ�����ֵ����Ũ����ֵ������k=
=
=4��
��μӷ�Ӧ��H2���ʵ���Ϊnmol��
CO��g��+H2O��g��?H2��g��+CO2��g����
��ʼ��mol����0 1 1 1
ת����mol����n n n n
ƽ�⣨mol����n 1+n 1-n 1-n
����
=4�����n=0.154
��Ӧǰ�������������䣬����ƽ��ʱ�����������ܵ����ʵ���Ϊ1mol+1mol+1mol=3mol��
ƽ��������CO2���������Ϊ
��100%=28.2%��
��ʱƽ���ϵ�CO2���������������27.55%��
�ʴ�Ϊ������Ӧ����B��
��3��ƽ�������������ƶ���
�ٲ��۸ı��������ƽ�������������ƶ�������������ʵ���һ�����ӣ��ʢ���ȷ��
�ڶ��ڶ���������뷴Ӧ����Ӧǰ��������������ķ�Ӧ���������д�������һ�ַ�Ӧ���ʹƽ�������ƶ�������������ʵ������ӣ����ٷֺ�����ȫ���Լ�С����Ϊ�������ˣ��ʢڴ���
�۶������ʲμӷ�Ӧ������һ�ַ�Ӧ���Ũ�ȣ�ƽ�������������ƶ������������Ӧ���ת���ʣ�����ת���ʽ��ͣ��ʢ۴���
�ܶ������ʲμӷ�Ӧ������һ�ַ�Ӧ���Ũ�ȣ�ƽ�������������ƶ���������Ӧ���Ũ�Ƚ��ͣ�����Ũ�����ʢܴ���
��ƽ�������������ƶ�������Ӧ����һ�������淴Ӧ���ʣ��ʢ���ȷ��
��ʹ�ô������ܸı�ƽ���ƶ����ʢ���
��ѡ���٢�
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ����mol�� 1 1 0 0
�仯����mol��
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
ƽ������mol��
| 1 |
| 3 |
| 1 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
��1����Ӧǰ�������������䣬����ƽ��ʱ�����������ܵ����ʵ���Ϊ1mol+1mol=2mol��
����ƽ��������CO2���������Ϊ=
| ||
| 2mol |
�ʴ�Ϊ��33.3%��
��2������1mol CO2��lmol H2��1mol H2O����Ӧ���淴Ӧ���н���ƽ�⣬��ЧΪ��1����ƽ����ټ�1molH2O��g����ƽ��������Ӧ�ƶ���
��ѧƽ�ⳣ��=������ƽ��Ũ��ϵ���η�֮���뷴Ӧ��ƽ��Ũ��ϵ���η�֮���ıȣ�
�ʸ÷�Ӧ��ƽ�ⳣ������ʽk=
| c(H2)c(CO2) |
| c(CO)c(H2O) |
| c(H2)c(CO2) |
| c(CO)c(H2O) |
| ||||
|
��μӷ�Ӧ��H2���ʵ���Ϊnmol��
CO��g��+H2O��g��?H2��g��+CO2��g����
��ʼ��mol����0 1 1 1
ת����mol����n n n n
ƽ�⣨mol����n 1+n 1-n 1-n
����
| (1-n)(1-n) |
| n(1+n) |
��Ӧǰ�������������䣬����ƽ��ʱ�����������ܵ����ʵ���Ϊ1mol+1mol+1mol=3mol��
ƽ��������CO2���������Ϊ
| 1mol-0.154mol |
| 3mol |
��ʱƽ���ϵ�CO2���������������27.55%��
�ʴ�Ϊ������Ӧ����B��
��3��ƽ�������������ƶ���
�ٲ��۸ı��������ƽ�������������ƶ�������������ʵ���һ�����ӣ��ʢ���ȷ��
�ڶ��ڶ���������뷴Ӧ����Ӧǰ��������������ķ�Ӧ���������д�������һ�ַ�Ӧ���ʹƽ�������ƶ�������������ʵ������ӣ����ٷֺ�����ȫ���Լ�С����Ϊ�������ˣ��ʢڴ���
�۶������ʲμӷ�Ӧ������һ�ַ�Ӧ���Ũ�ȣ�ƽ�������������ƶ������������Ӧ���ת���ʣ�����ת���ʽ��ͣ��ʢ۴���
�ܶ������ʲμӷ�Ӧ������һ�ַ�Ӧ���Ũ�ȣ�ƽ�������������ƶ���������Ӧ���Ũ�Ƚ��ͣ�����Ũ�����ʢܴ���
��ƽ�������������ƶ�������Ӧ����һ�������淴Ӧ���ʣ��ʢ���ȷ��
��ʹ�ô������ܸı�ƽ���ƶ����ʢ���
��ѡ���٢�
���������⿼�黯ѧƽ��ļ��㼰Ӱ�����أ��Ѷ��еȣ�ƽ�ⳣ��ֻ���¶�Ӱ�죬�¶Ȳ��䣬ƽ�ⳣ�����䣮

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
��֪��������
Fe��s��+
O2��g��=FeO��s����H1=-272kJ/mol
2Al��s��+
O2��g��=Al2O3��s����H2=-1675kJ/mol
��2Al��s��+3FeO��s��=Al2O3��s��+3Fe��s���ġ�H3���ǣ�������
Fe��s��+
| 1 |
| 2 |
2Al��s��+
| 3 |
| 2 |
��2Al��s��+3FeO��s��=Al2O3��s��+3Fe��s���ġ�H3���ǣ�������
| A��+859kJ/mol |
| B��-859kJ/mol |
| C��-1403kJ/mol |
| D��+1403kJ/mol |
���¡���ѹ�£�1molA��amolB��һ���ݻ��ɱ�������з������·�Ӧ��A��g��+2B��g��?2C��g���� һ��ʱ���ﵽƽ�⣬����bmolC��������˵������ȷ���ǣ�������
| A����v����A���T2v����C��ʱ���ɶ϶���Ӧ�Ѵ�ƽ�� |
| B����ʼʱ�̺ʹ�ƽ��������е�ѹǿ��Ϊ 1��1 |
| C������A��B��ת����֮��Ϊ1��2 |
| D������ʼʱ����2molA��2amolB�����ƽ��ʱ����2bmolC |
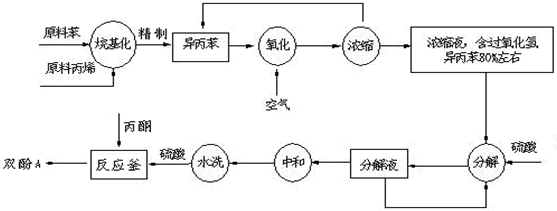
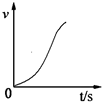 ��2�������������У���Ҫ�ϸ�����¶ȣ���ֹ�¶ȹ��ߣ���ԭ���ǣ��ٷ�ֹ��Ӧ���ھ��Ң�
��2�������������У���Ҫ�ϸ�����¶ȣ���ֹ�¶ȹ��ߣ���ԭ���ǣ��ٷ�ֹ��Ӧ���ھ��Ң� ij��ѧ��ȤС���ͬѧ������ͼ��ʾʵ��װ�ý���ʵ�飨ͼ��a��b��c��ʾֹˮ�У���
ij��ѧ��ȤС���ͬѧ������ͼ��ʾʵ��װ�ý���ʵ�飨ͼ��a��b��c��ʾֹˮ�У���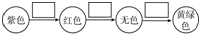
 ��ͼ��ʵ��������ϩ�ķ���װ�ú���ϩ����ʵ��װ�ã���Ӧԭ��Ϊ��
��ͼ��ʵ��������ϩ�ķ���װ�ú���ϩ����ʵ��װ�ã���Ӧԭ��Ϊ��