题目内容
20.5L 1mol/L的氯化钠溶液加热蒸发掉一部分溶剂,蒸发后测得体积变为1L且无晶体析出,则蒸发后溶液中氯化钠的物质的量浓度为多少?分析 溶液在蒸发过程中溶质的物质的量不变,根据n=cV计算出溶液中NaCl的物质的量,然后根据c=$\frac{n}{V}$计算出蒸发后溶液中氯化钠的物质的量浓度.
解答 解:5L 1mol/L的氯化钠溶液加热蒸发掉一部分溶剂,蒸发后测得体积变为1L且无晶体析出,则蒸发后溶液中氯化钠的物质的量为:1mol/L×5L=5mol,
蒸发后溶液中NaCl的物质的量浓度为:c(NaCl)=$\frac{5mol}{1L}$=5mol/L,
答:蒸发后溶液中氯化钠的物质的量浓度为5mol/L.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确蒸发前后溶质的物质的量不变为解答关键,注意掌握物质的量浓度的概念及表达式.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
10.下列除杂方案合理的是( )
| A. | 除去溴苯中少量的溴:加入苯萃取,分液 | |
| B. | 除去乙酸乙酯中的少量乙酸:加入饱和Na2CO3溶液,分液 | |
| C. | 除去乙烯中少量的SO2:气体通过盛有酸性高锰酸钾溶液的洗气瓶 | |
| D. | 除去MgCl2溶液中少量的FeCl3:加入稍过量氢氧化钠,过滤 |
11.从下列事实所得出的解释或结论正确的是( )
| 选项 | 实验事实 | 解释或结论 |
| A | 已建立平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动 | 反应物的浓度一定降低 |
| B | 压缩针筒内的NO2和N2O4混合气体,颜色先变深后变浅 | 增大压强,平衡向生成N2O4的方向移动 |
| C | 由水电离出来的c(H+)=1.0×10-13mol/L溶液 | 该溶液为氯化铵水溶液 |
| D | 向含有NH4+、Mg2+、Cu2+、Al3+溶液中加入过量的氢氧化钠溶液微热并搅拌,再加过量的盐酸,其中NH4+大量减少 | NH4+水解 |
| A. | A | B. | B | C. | C | D. | D |
8.根据下表信息,判断0.10mol/L的下列各溶液pH值最大的是( )
| 酸 | 电离常数 |
| CH3COOH | Ki=1.8×10 -5 |
| H2CO3 | Ki1=4.3×10 -7,Ki2=5.6×10 -11 |
| H2S | Ki1=9.1×10 -8,Ki2=1.1×10 -12 |
| H3PO4 | Ki1=7.5×10 -3,Ki2=6.2×10 -8,Ki3=2.2×10 -13 |
| A. | CH3COONa | B. | Na2CO3 | C. | Na2S | D. | Na3PO4 |
2.下列说法正确的是( )
| A. | 胶体区别于其他分散系的本质特征是胶体可发生丁达尔效应 | |
| B. | 在一定温度和压强下,气体体积主要取决于气体分子之间的平均间距 | |
| C. | 道尔顿、阿伏伽德罗、卢瑟福、波尔等科学家的研究不断更新人们对原子结构的认识 | |
| D. | 确定物质中是否含有C、H、O、N、Cl、Br、S等元素可用元素分析仪,确定物质中是否含有哪些金属元素可用原子吸收光谱 |
9.下列有关实验的说法不正确的是( )
| A. | 用精密pH试纸测得某碱溶液的pH为12.3 | |
| B. | 用25mL酸式滴定管量取13.50mLK2Cr2O7溶液 | |
| C. | 测定中和热实验的玻璃仪器只需烧杯、量筒和温度计 | |
| D. | 用带橡皮塞的试剂瓶保存Na2CO3溶液 |
6.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 水电离出的c(H+)=10-12mol•L-1的溶液中:Na+、K+、Cl-、AlO2- | |
| B. | 0.1mol•L-1的HNO3溶液中:K+、[Ag(NH3)2]+、Cl- | |
| C. | 含有大量Fe3+的溶液中:Na+、H+、I-、SO42- | |
| D. | 澄清透明的溶液中:Cu2+、SO42-、Mg2+、Cl- |
7.设阿伏加德罗常数的数值为NA,下列说法正确的是( )
| A. | 室温下体积为10L、pH=13的NaOH溶液中含有Na+的数目为NA | |
| B. | 常温常压下,17g氨气中含有氢原子的数目为NA | |
| C. | 电解水时,阳极生成11.2L气体,则电路中通过的电子数为2NA | |
| D. | 体积为1L、物质的量浓度为1mol•L-1的Na2CO3溶液中含有NA个CO32- |
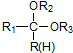 $\stackrel{H+/H_{2}O}{→}$
$\stackrel{H+/H_{2}O}{→}$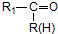
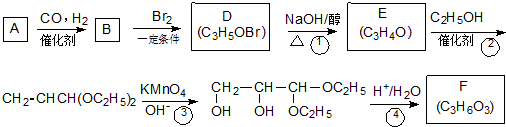
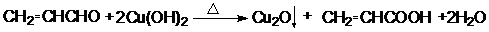 ;
;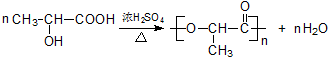 .
.