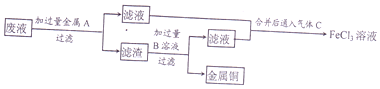
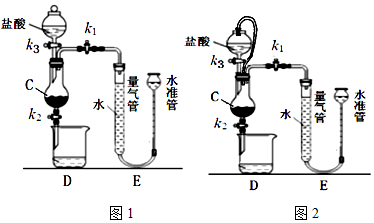
题目内容
20.在Al3++3H2O≒Al(OH)3+3H+的平衡体系中,要抑制Al3+的水解,可采取的措施为( )| A. | 加热 | B. | 通入氯化氢气体 | ||
| C. | 加入适量的氢氧化钠溶液 | D. | 加入固体AlCl3 |
分析 由Al3++3H2O≒Al(OH)3+3H+可知,加酸可抑制Al3+的水解,以此来解答.
解答 解:A.水解为吸热反应,加热促进水解,故A不选;
B.通入氯化氢气体,氢离子浓度增大,抑制水解,故B选;
C.加入适量的氢氧化钠溶液,与氢离子反应,促进水解,故C不选;
D.加入固体AlCl3,平衡正向移动,故D不选;
故选B.
点评 本题考查化学平衡移动,为高频考点,把握温度、浓度对化学平衡的影响为解答的关键,侧重分析与应用能力的考查,注意水解平衡移动的特点,题目难度不大.

练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
11.下列各物质相互混合进行反应,既有气体生成,最终又有白色沉淀生成的是( )
| A. | 金属钠投入CuSO4溶液中 | B. | 过量的NaOH溶液和明矾溶液反应 | ||
| C. | 金属钠投入MgSO4溶液中 | D. | 金属铝投入NaOH溶液中 |
8.配置一定物质的量浓度的NaCl溶液,不需要使用的仪器是( )
| A. | 烧杯 | B. | 容量瓶 | C. | 漏斗 | D. | 玻璃棒 |
11.在硫酸铜饱和溶液中,投入不规则的硫酸铜晶体,下列说法正确的是( )
| A. | 晶体形状不变 | B. | 晶体溶解,溶液的浓度变大 | ||
| C. | 晶体不溶解,溶液浓度不变 | D. | 晶体形状改变,溶液浓度不变 |
8.有两个无标签的试剂瓶,分别装有Na2CO3和NaHCO3固体,有4位同学为鉴别它们采用了以下不同的方法,其中不可行的是( )
| A. | 分别配成溶液,再加入澄清石灰水 | |
| B. | 分别取固体样品,滴加同浓度盐酸,观察产生气泡的快慢 | |
| C. | 分别加热,再检验是否有使澄清石灰水变浑浊的气体产生 | |
| D. | 在两只试管中分别加入各约1 g的两种固体和10 mL水,振荡后分别滴入2滴酚酞 |
9.短周期主族元素X、Y、Z、W的原子序数依次增大,X元素原子最外层电子数是内层的2倍,Z是地壳中含量最高的元素,W是同周期原子半径最大的金属元素.下列说法正确的是( )
| A. | 原子半径的大小顺序:r(W)>r(Z)>r(Y) | |
| B. | X的最高价氧化物对应水化物的酸性比Y的强 | |
| C. | Z的简单气态氢化物的热稳定性比Y的强 | |
| D. | Z分别与X、W形成的化合物的化学键类型相同 |