题目内容
3.分子式为C7H8O2并能与金属钠反应的芳香化合物有( )| A. | 9种 | B. | 10种 | C. | 11种 | D. | 12种 |
分析 C7H8O2的不饱和度为4,为芳香化合物,含有苯环,能与钠反应,含有-OH,侧链为-OH、-OCH3,有邻、间、对三种,侧链为-OH、-CH2OH,有邻、间、对三种,侧链为2个-OH、1个-CH3,2个-OH有邻、间、对三种,结合等效氢判断.
解答 解:C7H8O2的不饱和度为4,为芳香化合物,含有苯环,能与钠反应,含有-OH,侧链为-OH、-OCH3,有邻、间、对三种,侧链为-OH、-CH2OH,有邻、间、对三种,侧链为2个-OH、1个-CH3,2个-OH为邻位时,-CH3有2种位置,2个-OH为间位时,-CH3有3种位置,2个-OH为对位时,-CH3有1种位置,故符合条件的同分异构体有3+3+2+3+1=12种,
故选:D.
点评 本题考查同分异构体书写,注意利用定二移一法确定苯环三元取代同分异构体数目,难度中等.

练习册系列答案
相关题目
13.若mg Na在足量氯气中燃烧,生成固体的质量为(m+3.55g),则mg Na与氧气反应,生成固体的质量为 ( ) ①(m+0.8g) ②(m+1.0g) ③(m+1.2g) ④(m+1.6g) ⑤(m+1.4g)
| A. | ①②④ | B. | ①⑤ | C. | ③④ | D. | ①②③④⑤ |
11.火箭推进器常以联氨(N2H4) 为燃料、过氧化氢为助燃剂.已知下列各物质反应的热化学方程式:N2H4(g)+O2(g)═N2(g)+2H2O(g)△H1=-533.23kJ•mol-1
H2O(g)═H2O (l)△H2=-44kJ•mol-1
2H2O2(l)═2H2O(l)+O2(g)△H3=-196.4kJ•mol-1
则联氨与过氧化氢反应的热化学方程式可表示为( )
H2O(g)═H2O (l)△H2=-44kJ•mol-1
2H2O2(l)═2H2O(l)+O2(g)△H3=-196.4kJ•mol-1
则联氨与过氧化氢反应的热化学方程式可表示为( )
| A. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(l)△H=+817.63 kJ•mol-1 | |
| B. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.63 kJ•mol-1 | |
| C. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(l)△H=-641.63 kJ•mol-1 | |
| D. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=-817.63 kJ•mol-1 |
8.如图所示装置是一种可充电电池示意图,装置中的离子交换膜只允许Na+通过.已知充放电的化学方程式为:2Na2S2+NaBr3$?_{充电}^{放电}$Na2S4+3NaBr.下列说法正确的是( )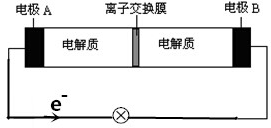

| A. | 放电时,Na+从右到左通过离子交换膜 | |
| B. | 放电时,负极反应式为3NaBr-2e-═NaBr3+2Na+ | |
| C. | 充电时,A极应与直流电源负极相连 | |
| D. | 放电时,当有0.1molNa+通过离子交换膜时,B极上有0.3molNaBr产生 |
15.下列说法中,正确的是( )
| A. | 甲醛、乙醛、丙醛通常情况下都是液体 | |
| B. | 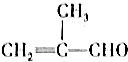 是乙醛的同系物 是乙醛的同系物 | |
| C. | 可用浓盐酸洗去银镜反应实验生成的银镜 | |
| D. | 1mol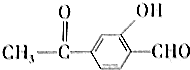 最多能与5mol H2发生反应 最多能与5mol H2发生反应 |
8.下列说法正确的是( )
| A. | 铝在空气中耐腐蚀,所以铝是不活泼金属 | |
| B. | 铝能与冷水反应 | |
| C. | 铝热反应常用于冶炼某些熔点较高的金属 | |
| D. | 冶炼铝可用电解AlCl3的方法 |
9.下列选项中,为完成相应实验,所用仪器、试剂及相关操作合理的是( )
| A. | 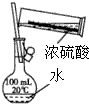 稀释浓硫酸 | |
| B. | 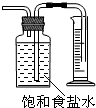 测量Cl2的体积 | |
| C. | 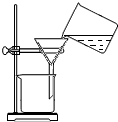 过滤 | |
| D. | 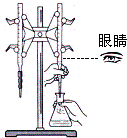 用NaOH标准溶液滴定锥形瓶中的盐酸 |