题目内容
根据元素周期表和元素周期律分析下面的推断,其中错误的是( )
| A、锂(Li)的原子失电子能力比钠弱 |
| B、砹(At)的氢化物不稳定 |
| C、H2S比水稳定 |
| D、氢氧化钠比氢氧化镁的碱性强 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:A.同主族自上而下金属性增强,失去电子能力增强;
B.同主族自上而下非金属性减弱,氢化物稳定性减弱;
C.同主族自上而下非金属性减弱,氢化物稳定性减弱;
D.金属性越强,最高价氧化物对应水化物的碱性越强.
B.同主族自上而下非金属性减弱,氢化物稳定性减弱;
C.同主族自上而下非金属性减弱,氢化物稳定性减弱;
D.金属性越强,最高价氧化物对应水化物的碱性越强.
解答:
解:A.Li、Na同主族,自上而下金属性增强,失去电子能力增强,故锂(Li)的原子失电子能力比钠弱,故A正确;
B.同主族自上而下非金属性减弱,氢化物稳定性减弱,非金属性At<I,砹(At)的氢化物稳定性比较HI弱,而HI易分解,则砹(At)的氢化物不稳定,故B正确;
C.同主族自上而下非金属性减弱,氢化物稳定性减弱,故水比H2S稳定,故C错误;
D.同周期自左而右金属性增强,故金属性Na>Mg,金属性越强,最高价氧化物对应水化物的碱性越强,故氢氧化钠碱性比氢氧化镁强,故D正确,
故选C.
B.同主族自上而下非金属性减弱,氢化物稳定性减弱,非金属性At<I,砹(At)的氢化物稳定性比较HI弱,而HI易分解,则砹(At)的氢化物不稳定,故B正确;
C.同主族自上而下非金属性减弱,氢化物稳定性减弱,故水比H2S稳定,故C错误;
D.同周期自左而右金属性增强,故金属性Na>Mg,金属性越强,最高价氧化物对应水化物的碱性越强,故氢氧化钠碱性比氢氧化镁强,故D正确,
故选C.
点评:本题考查同周期、同主族元素化合物性质递变规律,比较基础,侧重对基础知识的巩固.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法正确的是( )
| A、25℃,NaHCO3在水中的溶解度比Na2CO3的小 |
| B、Na2O和Na2O2中的阴阳离子个数比不相等 |
| C、用洁净铂丝蘸取溶液进行焰色反应,火焰呈黄色说明原溶液中有Na+无K+ |
| D、Na与足量O2反应,随温度升高生成Na2O的速率逐渐加快 |
下列五种烃①异戊烷②新戊烷③戊烷④丙烷⑤丁烷,按沸点由高到低的顺序排列的是( )
| A、①>②>③>④>⑤ |
| B、②>③>⑤>④>① |
| C、③>①>②>⑤>④ |
| D、④>⑤>②>①>③ |
化学与工农业生产和人类生活密切相关.下列说法错误的是( )
| A、2013年1月1日起,我国正式发布环境空气质量指数(AQI),包括PM2.5、PM10、O3、CO2、SO2和NO2等6项指标 |
| B、生石灰、硅胶是食品包装中常用的干燥剂 |
| C、“雨后彩虹”是与胶体、光学等知识有关的自然现象 |
| D、为防止月饼等富脂食品氧化变质,常在包装袋中放入硫酸亚铁 |
一定条件下,在容积不变的密闭容器中加入P、Q进行反应P(g)+2Q(g)═3R(g)+S(l),说明该反应已达到平衡的是( )
| A、反应容器中气体的平均摩尔质量不再改变 |
| B、反应容器中P、Q、R、S四者共存 |
| C、2v正(Q)=3 v逆(R) |
| D、反应容器中压强不随时间变化而变化 |
 直接排放煤燃烧产生的烟气会引起严重的环境问题,将烟气通过装有石灰石浆液的脱硫装置可以除去其中的二氧化硫,最终生成硫酸钙.硫酸钙可在图中所示的循环燃烧装置的燃料反应器中与甲烷反应,气体产物分离出水后得到几乎不含杂质的二氧化碳,从而有利于二氧化碳的回收利用,达到减少碳排放的目的.
直接排放煤燃烧产生的烟气会引起严重的环境问题,将烟气通过装有石灰石浆液的脱硫装置可以除去其中的二氧化硫,最终生成硫酸钙.硫酸钙可在图中所示的循环燃烧装置的燃料反应器中与甲烷反应,气体产物分离出水后得到几乎不含杂质的二氧化碳,从而有利于二氧化碳的回收利用,达到减少碳排放的目的.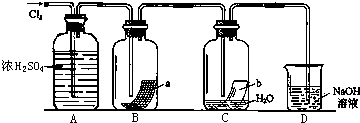 为验证干燥的Cl2没有漂白性,而Cl2与水反应后的产物具有漂白性,肖飞同学设计了如下实验.(其中a是有色布条)
为验证干燥的Cl2没有漂白性,而Cl2与水反应后的产物具有漂白性,肖飞同学设计了如下实验.(其中a是有色布条)