题目内容
8.下列说法正确的是( )
| A. | 构成原电池的两个电极必须是活泼性不同的两种金属 | |
| B. | 右图原电池中,电流由锌棒经外电路流向铜棒 | |
| C. | 通过构成原电池,能将反应的化学能全部转化为电能 | |
| D. | 银锌纽扣电池的放电反应:Zn+Ag2O+H2O=Zn(OH)2+2Ag,其中Ag2O作正极,发生还原反应 |
分析 A.两个电极中,可以一极为较活泼金属,另一极为石墨棒;
B.电流从原电池正极流向负极,锌为负极,铜为正极;
C.原电池是将化学能转化成电能的装置,但是能量的转化率不可能为100%;
D.根据化合价变化可知Ag元素化合价降低被还原,应为原电池的正极,在正极上发生还原反应.
解答 解:A.构成原电池的两个电极不一定都是金属,可以是一极为较活泼金属,另一极为石墨棒,故A错误;
B.该原电池中,锌为负极,铜为正极,电流由铜棒经外电路流向锌棒,故B错误;
C.通过构成原电池,能将反应的化学能转化为电能,由于存在能量损失,则不可能将化学能全部转化为电能,故C错误;
D.由电池总反应可知该纽扣电池的反应中Zn为还原剂、Ag2O为氧化剂,故Zn为负极被氧化、Ag2O为正极被还原,发生还原反应,故D正确;
故选D.
点评 本题考查了原电池工作原理,题目难度中等,明确原电池工作原理为解答关键,注意掌握判断原电池两极的方法,试题有利于提高学生的灵活应用能力.

练习册系列答案
相关题目
18. 科学家对石墨进行处理,使得石墨片的厚度逐渐减少,最终获得目前已知的最薄的材料--石墨烯(如图).下列关于石墨烯的说法正确的是( )
科学家对石墨进行处理,使得石墨片的厚度逐渐减少,最终获得目前已知的最薄的材料--石墨烯(如图).下列关于石墨烯的说法正确的是( )
 科学家对石墨进行处理,使得石墨片的厚度逐渐减少,最终获得目前已知的最薄的材料--石墨烯(如图).下列关于石墨烯的说法正确的是( )
科学家对石墨进行处理,使得石墨片的厚度逐渐减少,最终获得目前已知的最薄的材料--石墨烯(如图).下列关于石墨烯的说法正确的是( )| A. | 石墨烯是一新型的纳米化合物 | B. | 石墨烯与C60互为同素异形体 | ||
| C. | 石墨烯是一种有机物 | D. | 石墨烯中碳元素的化合价为+3 |
19.下列有关实验设计或对实验原理的描述正确的是( )
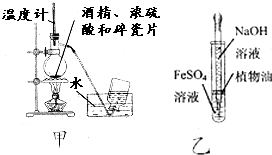

| A. | 为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体 | |
| B. | 用甲图装置制取乙烯 | |
| C. | 用乙图装置制备少量氢氧化亚铁 | |
| D. | 加入适量乙醇和浓硫酸,加热,可除去乙酸乙酯中少量的乙酸 |
3.下列表示正确的是( )
| A. | 乙炔分子球棍模型: | B. | Na+的结构示意图为: | ||
| C. | 硝基苯的结构简式: | D. | 羟基的电子式: |
13.下列说法正确的是( )
| A. | 在淀粉溶液中加入稀硫酸并加热数分钟,冷却后依次加入新制Cu(OH)2悬浊液和碘水,可检验淀粉是否水解 | |
| B. | 做过碘升华的圆底烧瓶可以用酒精洗涤 | |
| C. | 为了验证Na2CO3固体中是否含有NaHCO3,溶于水后加石灰水,看有无沉淀 | |
| D. | 用pH试纸测定溶液pH时,通常是将pH试纸放入待测溶液中润湿后,半分钟内跟标准比色卡比较 |
20.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 0.1mol乙烯和乙醇(蒸汽)混合物完全燃烧所消耗的氧分子数一定为0.3NA | |
| B. | 在反应KIO3+6HI=KI+3I2+3H2O中,每生成3molI2转移的电子数为6NA | |
| C. | 含4molSi-O键的二氧化硅晶体中,氧原子数为4NA | |
| D. | 120gNaHSO4固体中含有的离子总数为3NA |
10.下列关于安全事故的处理方法,正确的是( )
| A. | 金属钠着火时,立即用沾水的毛巾覆盖 | |
| B. | 不慎渗出的酒精在桌上着火时,立即用大量水扑灭 | |
| C. | 大量氯气泄漏时,迅速离开现场,并尽量往高处去 | |
| D. | 少量浓硫酸沾在皮肤上,立即用大量氢氧化钠溶液冲洗 |
11.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 25℃,pH=12的Na2CO3溶液中含有OH-的数目为0.01NA | |
| B. | 1mol苯乙烯中含有的碳碳双键数为4NA | |
| C. | 标准状况下,2.24L己烷中原子数为2NA | |
| D. | 通常状况下,18g水所含的中子数为8NA |



