题目内容
18.用NA表示阿伏加德罗常数的值,下列叙述不正确的是( )| A. | 标准状况下,6.72LO2和N2的混合气体含有的原子数为0.6NA | |
| B. | 通常状况下,8g O2和O3 的混合气体含有的分子数是0.5NA | |
| C. | 常温常压下,2mol/L的100mL MgCl2溶液中,含有Cl- 个数为0.4NA | |
| D. | 标准状况下,11.2L H2在氧气中完全燃烧后得到的产物的分子数为0.5NA |
分析 A.依据n=$\frac{V}{Vm}$计算混合气体的物质的量,结合氧气和氮气都是双原子分子解答;
B.依据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$计算;
C.依据n=CV计算氯化镁的物质的量,氯化镁为强电解质,1mol氯化镁电离产生2mol氯离子;
D.依据方程式:2H2+O2=2H2O计算解答.
解答 解:A.氧气和氮气都是双原子分子,标准状况下,6.72LO2和N2的混合气体物质的量$\frac{6.72L}{22.4L/mol}$=0.3mol,含有原子物质的量为0.6mol,含有的原子数为0.6NA,故A正确;
B.氧气和臭氧摩尔质量不同,所以相同质量的氧气和臭氧物质的量不同,含有的分子数不同,故B错误;
C.常温常压下,2mol/L的100mL MgCl2溶液中含有氯化镁含有物质的量为2mol/L×0.1L=0.2mol,含有Cl- 个数为0.2mol×2NA=0.4NA,故C正确;
D.标准状况下,11.2L H2物质的量为$\frac{11.2L}{22.4L/mol}$=0.5mol,依据2H2+O2=2H2O,可知在氧气中完全燃烧后得到的产物的分子数为0.5NA,故D正确;
故选:B.
点评 本题考查了阿伏伽德罗常数及相关计算,熟悉以物质的量为核心的计算公式,明确气体摩尔体积使用条件和对象是解题关键,题目难度不大.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
9.已知AgCl在水中有以下溶解平衡:AgCl(s)?Ag+(aq)+Cl-(aq).将AgCl分别投入下列溶液中:
①40mL 0.03mol/L的盐酸;
②50mL 0.03mol/L的硝酸银溶液;?
③30mL 0.02mol/L的氯化钙溶液;
④10mL蒸馏水.
AgCl在四种溶液中的溶解度顺序为( )
①40mL 0.03mol/L的盐酸;
②50mL 0.03mol/L的硝酸银溶液;?
③30mL 0.02mol/L的氯化钙溶液;
④10mL蒸馏水.
AgCl在四种溶液中的溶解度顺序为( )
| A. | ?④>①=②>③ | B. | ?④>①>②=③ | C. | ?④=①>②>③ | D. | ?①=②>④>③ |
6.在不同温度下,将2mol X、2mol Y分别充入到不同体积的容器中,发生反应:X(g)+Y (g)?mZ(g)△H,所得Z的平衡浓度如表所示,下列说法正确的是( )
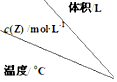 | 1 | 2 | 3 |
| 200 | $\frac{8}{3}$ | $\frac{4}{3}$ | $\frac{8}{9}$ |
| 300 | 2.4 | 1.2 | 0.8 |
| 400 | 2.0 | 1.0 | $\frac{2}{3}$ |
| A. | m=2,△H>0 | |
| B. | 300℃时,该反应平衡常数 K=9 | |
| C. | 在3L容器中进行反应,达到平衡的时间:400℃>200℃ | |
| D. | 200℃,2L容器中反应达平衡后,再充入2 mol Z,平衡时 Z 的体积分数增大 |
3.人们研究发现金星大气中有一种称之为硫化羰(COS)的分子,其结构与CO2类似,硫化羰是一种与生命密切相关的物质,下列有关COS的推测肯定不正确的是( )
| A. | COS分子中所有原子都满足8电子稳定结构 | |
| B. | COS与CO2互为等电子体 | |
| C. | COS分子是含有极性键的非极性分子 | |
| D. | COS的结构式为S=C=O |
10.当向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,烧杯中不可能出现的情况是( )
| A. | 溶液中有Fe2+和Cu2+ | B. | 溶液中只有Fe2+ | ||
| C. | 有铜粉无铁粉 | D. | 有铁粉无铜粉 |
7.下列中心原子的杂化轨道类型和分子几何构型均不正确的是( )
| A. | CCl4中C原子sp3杂化,为正四面体形 | |
| B. | BF3中B原子sp2杂化,为平面三角形 | |
| C. | CS2中C原子sp杂化,为直线形 | |
| D. | H2S分子中,S为sp杂化,为直线形 |