题目内容
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、标况下,2.24L乙醇含有0.2NA个碳原子 | ||
B、CO2通过Na2O2使其增重a g时,反应中转移的电子数为
| ||
| C、3.0gNO与1.12LO2(标况下)反应后,气体分子数可能为0.06NA | ||
| D、200mL2mol/L的NaOH溶液中,含有0.4NA个共价键 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、标准状况乙醇不是气体;
B、二氧化碳通过过氧化钠增重相当于为CO的质量;
C、一氧化氮和氧气反应生成二氧化氮,二氧化氮聚合生成四氧化二氮;
D、氢氧化钠溶液中含有水分子.
B、二氧化碳通过过氧化钠增重相当于为CO的质量;
C、一氧化氮和氧气反应生成二氧化氮,二氧化氮聚合生成四氧化二氮;
D、氢氧化钠溶液中含有水分子.
解答:
解:A、标准状况乙醇不是气体,2.24L乙醇物质的量不是0.1mol,故A错误;
B、二氧化碳通过过氧化钠增重相当于为CO的质量,每增重28gCO电子转移1mol,反应中转移的电子数为
NA,故B错误;
C、一氧化氮和氧气反应生成二氧化氮,二氧化氮聚合生成四氧化二氮,3.0gNO物质的量=
=0.1mol,与1.12LO2(标况下)物质的量=
=0.05mol,反应后,2NO+O2=2NO2,2NO2=N2O4,生成二氧化氮物质的量小于0.1mol,气体分子数可能为0.06,故C正确;
D、氢氧化钠溶液中含有水分子,200mL2mol/L的NaOH溶液中,含有共价键大于0.4NA个,故D错误;
故选C.
B、二氧化碳通过过氧化钠增重相当于为CO的质量,每增重28gCO电子转移1mol,反应中转移的电子数为
| a |
| 28 |
C、一氧化氮和氧气反应生成二氧化氮,二氧化氮聚合生成四氧化二氮,3.0gNO物质的量=
| 3.0g |
| 30/mol |
| 1.12L |
| 22.4L/mol |
D、氢氧化钠溶液中含有水分子,200mL2mol/L的NaOH溶液中,含有共价键大于0.4NA个,故D错误;
故选C.
点评:本题考查了阿伏伽德罗常数的分析判断,主要是气体摩尔体积条件应用,氧化还原反应电子转移,注意二氧化氮与四氧化二氮的化学平衡,题目较简单.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
下列过程所发生的化学变化属于取代反应的是( )
| A、苯与液溴在FeBr3催化作用下反应 |
| B、苯与氢气在镍做催化剂的条件下反应 |
| C、乙烯使酸性高锰酸钾褪色 |
| D、乙醇在铜做催化剂的条件下生成乙醛 |
下列说法正确的是( )
| A、化合反应一定是放热反应 |
| B、分解反应一定是吸热反应 |
| C、在化学反应过程中,发生物质变化的同时不一定发生能量变化 |
| D、破坏生成物全部化学键所需要的能量大于破坏反应物全部化学键所需要的能量时,反应为放热反应 |
下列说法中正确的是( )
| A、常温下,淀粉遇I- 变蓝色 |
| B、油脂水解可得到氨基酸和甘油 |
| C、淀粉和纤维素的组成都是(C6H10O5)n,水解最终产物都是葡萄糖,纤维素具有醇的性质,可以酯化 |
| D、糖类和蛋白质都是只由碳、氢、氧三种元素组成的有机物 |
实验是化学研究的基础.下列实验,不能达到实验目的是( )
A、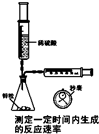 |
B、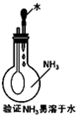 |
C、 |
D、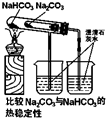 |
Na2CO3俗名纯碱,下面是对纯碱采用不同的分类法进行分类,其中不正确的是( )
| A、Na2CO3是碱 |
| B、Na2CO3是盐 |
| C、Na2CO3是钠盐 |
| D、Na2CO3是碳酸盐 |
设NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A、常温常压下,23克的NO2含有氧原子数为NA |
| B、25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| C、含NA个氧原子的O2与含NA个氧原子的O3的质量之比为3:2 |
| D、常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.2NA |