题目内容
实验是化学研究的基础.下列实验,不能达到实验目的是( )
A、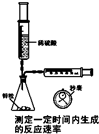 |
B、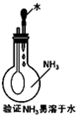 |
C、 |
D、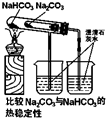 |
考点:化学实验方案的评价,中和热的测定,测定某些化学反应的速率,氨的制取和性质,探究碳酸钠与碳酸氢钠的性质
专题:实验评价题
分析:A.反应时,针筒确定气体体积,秒表确定时间;
B.挤压胶头滴管,氨气极易溶于水,内压减小;
C.图中缺少环形玻璃搅拌棒;
D.碳酸氢钠易分解,图中不能起对比作用.
B.挤压胶头滴管,氨气极易溶于水,内压减小;
C.图中缺少环形玻璃搅拌棒;
D.碳酸氢钠易分解,图中不能起对比作用.
解答:
解:A.反应时,针筒确定气体体积,秒表确定时间,由v=
可知,能测定反应速率,故A正确;
B.挤压胶头滴管,氨气极易溶于水,内压减小,可观察到气球变大,可验证氨气的溶解性,故B正确;
C.图中缺少环形玻璃搅拌棒,不能准确测定反应的最高温度,故C错误;
D.碳酸氢钠易分解,图中不能起对比作用,应在小试管中加碳酸氢钠,故D错误;
故选CD.
| △c |
| △t |
B.挤压胶头滴管,氨气极易溶于水,内压减小,可观察到气球变大,可验证氨气的溶解性,故B正确;
C.图中缺少环形玻璃搅拌棒,不能准确测定反应的最高温度,故C错误;
D.碳酸氢钠易分解,图中不能起对比作用,应在小试管中加碳酸氢钠,故D错误;
故选CD.
点评:本题考查化学实验方案的评价,为高频考点,涉及反应速率测定、氨气的溶解性、中和热测定、物质稳定性比较等,把握物质的性质及反应原理为解答的关键,注重高频考点的考查,注意实验装置图分析及实验操作的评价性分析,题目难度中等.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
下列除杂质的操作方法正确的是( )
| A、SO2中有少量的HCl:通过亚硫酸钠溶液 |
| B、碘晶体中有少量的NH4Cl:通过加热的方法 |
| C、NO中有少量的NO2:用水洗涤后再干燥 |
| D、Cl2中有少量的HCl:通过烧碱溶液 |
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、标况下,2.24L乙醇含有0.2NA个碳原子 | ||
B、CO2通过Na2O2使其增重a g时,反应中转移的电子数为
| ||
| C、3.0gNO与1.12LO2(标况下)反应后,气体分子数可能为0.06NA | ||
| D、200mL2mol/L的NaOH溶液中,含有0.4NA个共价键 |
下列各组离子,一定能在指定环境中大量共存的是( )
| A、含有大量I-离子的溶液中:Cl?、Fe3+、Al3+、Cu2+ |
| B、使甲基橙变红的溶液中:Fe3+、Na+、SO42-、NO3- |
| C、由水电离出的c(H+)=10-12 mol?L-1的溶液中:Na+、Ba2+、AlO2-、HCO3- |
| D、加入Al能放出大量H2的溶液中:NH4+、K+、SO32?、C1? |
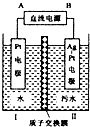 如图所示是利用电化学降解法治理水中的硝酸盐污染,电解槽中间用质子交换膜隔开,污水放入II区,通电使转NO3-化为N2,下面说法不正确的是( )
如图所示是利用电化学降解法治理水中的硝酸盐污染,电解槽中间用质子交换膜隔开,污水放入II区,通电使转NO3-化为N2,下面说法不正确的是( )| A、电解时H+从I区通过离子交换膜迁移到II区 |
| B、Ag-Pt电极上发生发应:2NO3-+10e-+6H2O═N2↑+12OH- |
| C、当电解过程中转移了1moL电子,则II区电解液质量减少2.8g |
| D、为增强溶液的导电性,I区水中可加入少量Na2SO4固体 |
下列微粒中,哪一组中的化学键含有非极性共价键( )
①C2H6 ②H2S ③CH2Cl2 ④NH4+.
①C2H6 ②H2S ③CH2Cl2 ④NH4+.
| A、①②③④ | B、只有① |
| C、只有①③ | D、只有②③ |
太阳能电池常用的主要材料是( )
| A、高纯硅 | B、活性炭 |
| C、铁合金 | D、金属钠 |