题目内容
Na2CO3俗名纯碱,下面是对纯碱采用不同的分类法进行分类,其中不正确的是( )
| A、Na2CO3是碱 |
| B、Na2CO3是盐 |
| C、Na2CO3是钠盐 |
| D、Na2CO3是碳酸盐 |
考点:酸、碱、盐、氧化物的概念及其相互联系
专题:物质的分类专题
分析:电离生成金属阳离子(或铵根离子)和酸根离子的化合物属于盐,根据盐中电离出的阳离子又可以将盐分为钾盐、钠盐、钡盐等,根据电离出的酸根离子可以将盐分为碳酸盐、硫酸盐、硝酸盐等.碱是电离出的阴离子全部是氢氧根离子的化合物.
解答:
解:A、碱电离生成的阴离子全部是氢氧根离子,则Na2CO3不是碱,属于盐,故A错误;
B、Na2CO3俗名纯碱,生成金属阳离子(或铵根离子)和酸根离子的化合物属于盐类,故B正确;
C、因阳离子为钠离子,故属于钠盐,故C正确;
D、因阴离子为碳酸根离子,则Na2CO3是碳酸盐,故D正确;
故选A.
B、Na2CO3俗名纯碱,生成金属阳离子(或铵根离子)和酸根离子的化合物属于盐类,故B正确;
C、因阳离子为钠离子,故属于钠盐,故C正确;
D、因阴离子为碳酸根离子,则Na2CO3是碳酸盐,故D正确;
故选A.
点评:本题考查学生盐的概念和分类知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、标况下,2.24L乙醇含有0.2NA个碳原子 | ||
B、CO2通过Na2O2使其增重a g时,反应中转移的电子数为
| ||
| C、3.0gNO与1.12LO2(标况下)反应后,气体分子数可能为0.06NA | ||
| D、200mL2mol/L的NaOH溶液中,含有0.4NA个共价键 |
下列各组离子,一定能在指定环境中大量共存的是( )
| A、含有大量I-离子的溶液中:Cl?、Fe3+、Al3+、Cu2+ |
| B、使甲基橙变红的溶液中:Fe3+、Na+、SO42-、NO3- |
| C、由水电离出的c(H+)=10-12 mol?L-1的溶液中:Na+、Ba2+、AlO2-、HCO3- |
| D、加入Al能放出大量H2的溶液中:NH4+、K+、SO32?、C1? |
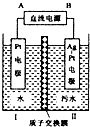 如图所示是利用电化学降解法治理水中的硝酸盐污染,电解槽中间用质子交换膜隔开,污水放入II区,通电使转NO3-化为N2,下面说法不正确的是( )
如图所示是利用电化学降解法治理水中的硝酸盐污染,电解槽中间用质子交换膜隔开,污水放入II区,通电使转NO3-化为N2,下面说法不正确的是( )| A、电解时H+从I区通过离子交换膜迁移到II区 |
| B、Ag-Pt电极上发生发应:2NO3-+10e-+6H2O═N2↑+12OH- |
| C、当电解过程中转移了1moL电子,则II区电解液质量减少2.8g |
| D、为增强溶液的导电性,I区水中可加入少量Na2SO4固体 |
下列物质不能以食盐为原料而生产的是( )
| A、盐酸 | B、硫酸 | C、烧碱 | D、纯碱 |
下列微粒中,哪一组中的化学键含有非极性共价键( )
①C2H6 ②H2S ③CH2Cl2 ④NH4+.
①C2H6 ②H2S ③CH2Cl2 ④NH4+.
| A、①②③④ | B、只有① |
| C、只有①③ | D、只有②③ |
对于可逆反应N2+3H2
2NH3达到平衡时,下列说法正确的是( )
| ||
| 高温高压 |
| A、N2、NH3、H2三种物质的浓度一定相等 |
| B、N2、H2全部变成NH3 |
| C、反应混合物各组分的浓度不再变化 |
| D、反应已经停止 |
在下列物质中,属于离子化合物的是( )
| A、HCl |
| B、H2O |
| C、NaCl |
| D、Cl2 |