题目内容
16.写出下列物质间转化的化学方程式,并注明反应条件CH3CHO←C2H50H←C2H4→C2H5Br
(1)C2H4→C2H5BrCH2=CH2+HBr→CH3CH2Br
(2)C2H4→C2H50HCH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH,
(3)C2H5OH→CH3CHO2CH3CH2OH+O2$→_{△}^{铜}$2CH3CHO+2H2O.
分析 (1)乙烯与溴化氢加成生成溴乙烷;
(2)乙烯与水加成生成乙醇;
(3)乙醇催化氧化生成乙醛和水.
解答 解:(1)发生加成反应生成溴乙烷,反应为CH2=CH2+HBr→CH3CH2Br,属于加成反应,
故答案为:CH2=CH2+HBr→CH3CH2Br;
(2)CH2=CH2中含有不饱和的C=C双键,能够在催化剂存在条件下与水发生加成反应生成乙醇,反应的化学方程式为:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH,
故答案为:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH;
(3)乙醇含有羟基,可发生催化氧化生成乙醛,方程式为2CH3CH2OH+O2$→_{△}^{铜}$2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{铜}$2CH3CHO+2H2O.
点评 本题考查有机物的机构和性质,为高考常见题型,注意把握有机物的官能团的性质以及相关方程式的书写,为解答该题的关键.

练习册系列答案
相关题目
7.某无色溶液能溶解Al(OH)3,则此溶液中一定能大量共存的离子组是( )
| A. | Fe2+、Cl-、Na+、NO3- | B. | K+ Na+、NO3-、HCO3- | ||
| C. | Na+、Ba2+、Cl-、NO3- | D. | Na+、K+、[Al(OH)4]-、SO42- |
4.具有下列电子排布式的原子中,半径最大的是( )
| A. | ls22s22p63s23p5 | B. | 1s22s22p3 | C. | 1s22s22p4 | D. | 1s22s22p63s23p3 |
11.下列属于吸热反应的是( )
| A. | 酸碱中和 | B. | 氢气燃烧 | ||
| C. | 浓硫酸的稀释 | D. | Ba(OH)2•8H2O和NH4Cl(固体)混合 |
1.将过量的CO2分别通入下列溶液中,最终有沉淀析出的溶液是( )
①CaCl2溶液 ②澄清石灰水 ③Ca(ClO)2溶液 ④饱和Na2CO3溶液.
①CaCl2溶液 ②澄清石灰水 ③Ca(ClO)2溶液 ④饱和Na2CO3溶液.
| A. | ①②③④ | B. | 只有②④ | C. | 只有①②③ | D. | 只有④ |
8.下列物质中,酸性最强的是( )
| A. | H2SiO3 | B. | H3PO4 | C. | H2SO4 | D. | HClO |
5.某强酸性溶液X中仅含有NH4+、Al3+、Ba2+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行连续实验,实验过程如图:下列有关推断不合理的是( )
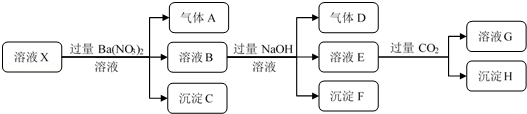

| A. | 根据上述连续实验不能确定溶液X中是否含有Fe3+ | |
| B. | 沉淀H为Al(OH)3 | |
| C. | 溶液中一定含有H+、Al3+、NH4+、Fe2+、SO42-、Cl- | |
| D. | 若溶液X为100 mL,产生的气体A为112 mL(标况),则X中c(Fe2+)=0.15 mol•L |
 ,加聚反应.
,加聚反应.