题目内容
1.某兴趣小组利用以下实验装置模拟工业炼铁的主要过程: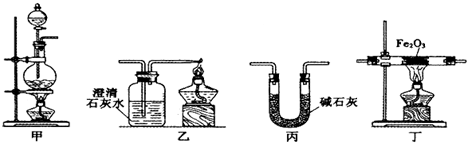
(1)装置甲中发生的反应为:HCOOH(甲酸)$→_{△}^{浓硫酸}$CO↑+H2O.已知甲酸是一种无色有刺激性气味的液体.制取一氧化碳时应该a(填字母).
a.将甲酸滴入浓硫酸 b.将浓硫酸滴入甲酸 c.将甲酸与浓硫酸混合后加入
(2)请按合适的顺序连接好以下装置:甲→丙→丁→乙
(3)丙装置中碱石灰的作用是除去一氧化碳中的甲酸和水蒸气.
(4)实验将近完成时,熄灭装置甲、乙、丁中酒精灯的先后顺序为丁甲乙.
(5)为了探究影响反应产物的外界因素,在Fe2O3与CO反应部位,该小组同学分别用酒精灯和酒精喷灯进行了两次实验,结果如下:
| 加热方式 | 通CO加热 时间/min | 澄清石灰水变 浑浊时间/min | 产物颜色 | 产物能否全部 被磁铁吸引 |
| 酒精灯 | 30 | 5 | 黑色 | 能 |
| 酒精喷灯 | 30 | 1 | 黑色 | 能 |
②丙同学查找资料发现,Fe3O4也能被磁铁吸引,对黑色产物成分提出以下三种假设:i.全部为铁;ii.全部为四氧化三铁;iii.四氧化三铁和铁的混合物.
分析 (1)装置甲中发生的反应为:HCOOH(甲酸)$→_{△}^{浓硫酸}$CO↑+H2O,制取一氧化碳时应该将甲酸滴入浓硫酸,不能将浓硫酸滴入甲酸中;
(2)根据制备CO,除杂、还原氧化铁、尾气处理连接装置;
(3)丙装置中碱石灰的作用是除杂;
(4)实验将近完成时,防止倒吸先熄灭装置丁中酒精灯,尾气处理最后熄灭;
(5)①因为产物能全部被磁铁吸引,所以不会有碳生成,又因为CO作还原剂化合价升高不可能生成碳单质,据此分析;
②根据Fe3O4也能被磁铁吸引,则组合可能为全部为铁,全部为Fe3O4,铁和Fe3O4都有.
解答 解:(1)装置甲中发生的反应为:HCOOH(甲酸)$→_{△}^{浓硫酸}$CO↑+H2O,因为甲酸具有挥发性,加热导致甲酸促进恢复,降低甲酸的利用率,所以制取一氧化碳时应该将甲酸滴入浓硫酸,故选:a;
(2)根据实验原理,应分为制备CO,除杂、还原氧化铁、尾气处理连接装置,所以顺序为甲丙丁乙,故答案为:丙;丁;乙;
(3)丙装置中碱石灰的作用是除杂,所以作用为除去CO中的甲酸和水蒸气,故答案为:除去CO中的甲酸和水蒸气;
(4)实验将近完成时,防止倒吸先熄灭装置丁中酒精灯,尾气处理最后熄灭,所以熄灭装置甲、乙、丁中酒精灯的先后顺序为丁甲乙,故答案为:丁甲乙;
(5)①因为产物能全部被磁铁吸引,所以不会有碳生成,又因为CO作还原剂化合价升高不可能生成碳单质,
故答案为:碳单质不会被磁铁吸引;CO作还原剂化合价升高不可能生成碳单质;
②根据Fe3O4也能被磁铁吸引,则组合可能为全部为铁,全部为Fe3O4,铁和Fe3O4都有,故答案为:全部为Fe3O4;铁和Fe3O4都有.
点评 本题考查了气体的制备及其工业炼铁的装置的选择等,题目涉及的知识点较多,侧重于基础知识的综合应用的考查,题目难度中等.

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案| A. | lmol葡萄糖能水解生成2molCH3CH2OH和2molCO2 | |
| B. | 苯的结构简式为 ,能使酸性高锰酸钾溶液褪色 ,能使酸性高锰酸钾溶液褪色 | |
| C. | 相同物质的量的乙烯与乙醇分别在足量的O2中完全燃烧,消耗O2的物质的量相同 | |
| D. | 乙烯和植物油都能使溴水褪色,其褪色原理不同 |
| A. | 某温度下,pH=7的NH4Cl与NH3•H2O的混合溶液:c(NH4+)=c(Cl-)>c(H+)=c(OH-) | |
| B. | 0.1 mol/L Na2S溶液:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| C. | 25℃时,pH=2的HCOOH与pH=12的NaOH等体积混合:c(HCOO-)<c(Na+) | |
| D. | 0.1 mol/L Na2CO3溶液与0.1 mol/L NaHCO3溶液等体积混合:3c(CO32-)+3c(HCO3-)+3c(H2CO3)=2c(Na+) |
| A. | pH=l 的溶液中:Ba2+、Fe3+、Cl-、SCN- | |
| B. | 能使酚酞变红的溶液:Ca2+、K+、HCO3-、CO32- | |
| C. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=10-12的溶液中:NH4+、Cu2+、NO3-、SO42- | |
| D. | 由水电离的c(H+)=10-12mol•L-1的溶液中:Na+、Al3+、Cl-、NO3- |
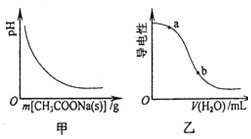
| A. | 图甲表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化 | |
| B. | 图乙表示向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b | |
| C. | 醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-) | |
| D. | 0.10 mol•L-1的CH3COOH溶液中加水稀释,溶液中c(OH-)减小 |
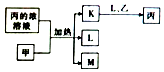 短周期主族元素W、X、Y、Z的原子序数依次增加,K、L、M均是由这些元素组成的二元化合物,甲、乙分别是元素X、Y的单质,甲是常见的固体,乙是常见的气体.K是无色气体,是主要的大气污染物之一,0.05mol/L丙溶液的pH为l,上述物质的转化关系如图所示.下列说法正确的是( )
短周期主族元素W、X、Y、Z的原子序数依次增加,K、L、M均是由这些元素组成的二元化合物,甲、乙分别是元素X、Y的单质,甲是常见的固体,乙是常见的气体.K是无色气体,是主要的大气污染物之一,0.05mol/L丙溶液的pH为l,上述物质的转化关系如图所示.下列说法正确的是( )| A. | 原子半径:W<X<Y | B. | 元素的非全属性:Z>Y>X | ||
| C. | 化合物XYZ中只含共价键 | D. | K、L、M中沸点最高的是M |