题目内容
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、1L 1mol?L-1的Na2SO4 溶液中含有的氧原子数为4NA |
| B、78g苯含有C=C双键的数目为3NA |
| C、常温常压下,28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA |
| D、标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.硫酸钠溶液中,水中含有氧原子,无法计算溶液中氧原子数目;
B.苯中的碳碳键为一种介于单键和双键之间的独特键,不存在碳碳双键;
C.烯烃和环丁烷的最简式为CH2,根据最简式计算出混合气体中含有碳原子的数目;
D.二氧化氮与水反应生成硝酸和一氧化氮,0.3mol二氧化氮与水反应生成0.1mol硝酸和0.2mol一氧化氮.
B.苯中的碳碳键为一种介于单键和双键之间的独特键,不存在碳碳双键;
C.烯烃和环丁烷的最简式为CH2,根据最简式计算出混合气体中含有碳原子的数目;
D.二氧化氮与水反应生成硝酸和一氧化氮,0.3mol二氧化氮与水反应生成0.1mol硝酸和0.2mol一氧化氮.
解答:
解:A.由于磷酸钠溶液中,溶剂水中也含有氧原子,所以无法计算溶液中氧原子的数目,故A错误;
B.78g苯的物质的量为1mol,苯分子中的碳碳键为一种独特键,苯分子中不存在碳碳双键,故B错误;
C.28g乙烯和环丁烷的混合物中含有2mol最简式CH2,含有2mol碳原子,混合气体中含有的碳原子数为2NA,故C正确;
D.标况下6.72L二氧化氮的物质的量为0.3mol,0.3mol二氧化氮与水完全反应生成0.2mol硝酸,转移了0.2mol电子,分反应转移的电子数目为0.2NA,故D错误;
故选C.
B.78g苯的物质的量为1mol,苯分子中的碳碳键为一种独特键,苯分子中不存在碳碳双键,故B错误;
C.28g乙烯和环丁烷的混合物中含有2mol最简式CH2,含有2mol碳原子,混合气体中含有的碳原子数为2NA,故C正确;
D.标况下6.72L二氧化氮的物质的量为0.3mol,0.3mol二氧化氮与水完全反应生成0.2mol硝酸,转移了0.2mol电子,分反应转移的电子数目为0.2NA,故D错误;
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确苯分子中的碳碳键为一种独特键,不存在碳碳双键,要求学生掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项A为易错点,注意水中含有氧原子.

练习册系列答案
相关题目
某氨水的pH=X,某盐酸的pH=Y,已知X+Y=14,将上述氨水与盐酸等体积混合后,所得溶液中各种离子浓度的关系正确的是( )
| A、c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| B、c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
| C、c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D、c(NH4+)+c(H+)>c(Cl-)+c(OH-) |
下列化合物中,只存在共价键的是( )
| A、NaOH |
| B、H2O |
| C、NH4Cl |
| D、CaO |
如图化合物中,核磁共振氢谱只出现两组峰且峰面积之比为3:2的是( )
A、 |
B、 |
C、 |
D、 |
以下能级符号错误的是( )
| A、5s | B、3d | C、3f | D、6p |
25℃时,pH值都等于11的NaOH溶液和Na2CO3溶液,两溶液中水的电离程度大小( )
| A、相等 |
| B、Na2CO3溶液大 |
| C、NaOH溶液大 |
| D、无法比较 |
常温下体积相同的下列四种溶液:①pH=3的盐酸②pH=3的醋酸溶液③pH=11的氨水④pH=11的NaOH溶液.下列说法中,正确的是( )
| A、②和④混合,所得混合溶液的pH大于7 |
| B、将四种溶液分别稀释到体积为原的100倍,溶液pH大小顺序③>④>②>① |
| C、③和④分别与足量稀硫酸中和,消耗硫酸的体积③=④ |
| D、①和③混合,所得混合溶液中c(H+)+c(NH4+)=c(Cl-)+c(OH-) |
下列有关NH3的尾气处理装置正确的是( )
A、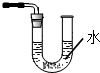 |
B、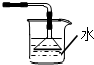 |
C、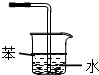 |
D、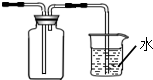 |
下列物质中不属于硅酸盐的是( )
| A、陶瓷 | B、玻璃 | C、水晶 | D、水泥 |