题目内容
下列有关NH3的尾气处理装置正确的是( )
A、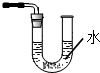 |
B、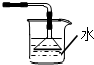 |
C、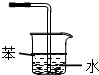 |
D、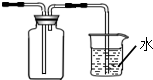 |
考点:尾气处理装置
专题:化学实验基本操作
分析:氨气极易溶于水,吸收氨气时不能直接将导管插入水中,必须使用防止倒吸的装置;常用的方法为:使用倒置的漏斗、使用球形漏斗、使用四氯化碳和水的混合液,据此进行判断.
解答:
解:A.该装置中,U型管左端通入氨气,能够防止倒吸,可用于吸收氨气,故A正确;
B.漏斗不能完全伸入液面中,否则无法起到防止倒吸的效果,正确的方法应该为: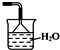 ,故B错误;
,故B错误;
C.导管直接伸入水中吸收氨气,会发生倒吸现象,可以使用四氯化碳和水的混合液吸收氨气,如: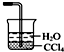 ,故C错误;
,故C错误;
D.集气瓶中应该采用“短进长出”方式,即进气导管应该短、出气管应该长,且插入烧杯中的导管稍稍伸入水中,才能起到防止倒吸作用,否则无法防止倒吸,不能用于吸收氨气,故D错误;
故选A.
B.漏斗不能完全伸入液面中,否则无法起到防止倒吸的效果,正确的方法应该为:
 ,故B错误;
,故B错误;C.导管直接伸入水中吸收氨气,会发生倒吸现象,可以使用四氯化碳和水的混合液吸收氨气,如:
 ,故C错误;
,故C错误;D.集气瓶中应该采用“短进长出”方式,即进气导管应该短、出气管应该长,且插入烧杯中的导管稍稍伸入水中,才能起到防止倒吸作用,否则无法防止倒吸,不能用于吸收氨气,故D错误;
故选A.
点评:本题考查了常见气体的尾气吸收,题目难度不大,注意明确常见的极易溶于水的气体在尾气吸收时,必须使用防止倒吸的装置,要求学生能够正确判断装置是否具有防止倒吸的作用.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
下列每组物质中含有的化学键类型相同的是( )
| A、NaCl、HCl、H2O、NaOH |
| B、Cl2、Na2S、HF、SO2 |
| C、HBr、CO2、NH3、H2O |
| D、Na2O2、H2O2、O3、CH4 |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、1L 1mol?L-1的Na2SO4 溶液中含有的氧原子数为4NA |
| B、78g苯含有C=C双键的数目为3NA |
| C、常温常压下,28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA |
| D、标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA |
一定条件下,在3L密闭容器中反应N2 (g)+3H2(g)?2NH3(g),10s后,氨气的物质的量增加了0.12mol,则前10s的平均反应速率为( )
| A、v(NH3)=0.003mol?L-1?s-1 |
| B、v(H2)=0.045mol?L-1?s-1 |
| C、v(H2)=0.006mol?L-1?s-1 |
| D、v(H2)=0.004mol?L-1?s-1 |
为证明溴乙烷分子中溴元素的存在,进行下列实验:
①加入AgNO3溶液 ②加入NaOH溶液
③加热 ④加蒸馏水
⑤加入稀HNO3溶液至溶液呈酸性 ⑥加入NaOH的乙醇溶液.
请指出实验操作步骤的合理顺序( )
①加入AgNO3溶液 ②加入NaOH溶液
③加热 ④加蒸馏水
⑤加入稀HNO3溶液至溶液呈酸性 ⑥加入NaOH的乙醇溶液.
请指出实验操作步骤的合理顺序( )
| A、②③⑤① | B、①②③④ |
| C、②③④⑤ | D、⑥③⑤① |
下列微粒的个数比不是1:1的是( )
| A、NaHCO3晶体中阴、阳离子 |
| B、NH3分子中的质子和电子 |
| C、14N原子中的质子和中子 |
| D、Na2O2固体中阴、阳离子 |
A、B为短周期元素,B3+比A2-离子少1个电子层,若A原子序数为n,则B的原子序数为( )
| A、n+5 | B、n+11 |
| C、n+3 | D、n-3 |
下列说法正确的是( )
| A、水的离子积常数KW只与温度有关,但外加酸、碱、盐一定会影响水的电离程度 | ||||
| B、Ksp不仅与难溶电解质的性质和温度有关,还与溶液中相关离子的浓度有关 | ||||
C、常温下,向10mL PH=3的醋酸溶液中加水稀释后,溶液中
| ||||
D、常温下,在0.10mol?L-1的NH3?H2O溶液中加入少量NH4Cl晶体,能使溶液的pH减小,
|
 B3N3H6是一种平面形分子(如图所示),因其分子结构的特殊性,被称为无机苯,“无机苯”的二氯代物的同分异构体的种类一共有( )
B3N3H6是一种平面形分子(如图所示),因其分子结构的特殊性,被称为无机苯,“无机苯”的二氯代物的同分异构体的种类一共有( )| A、3种 | B、4种 | C、5种 | D、6种 |