题目内容
11.某烷烃0.1mol完全燃烧,生成10.8gH2O和11.2LCO2(标准状况下)求:(1)该烷烃的分子式C5H12
(2)该烷烃的一种结构式
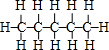 .
.
分析 计算水、二氧化碳的物质的量,根据原子守恒确定烷烃的分子式,进而书写可能的结构式.
解答 解:(1)某烷烃0.1mol完全燃烧,生成的物质的量为$\frac{10.8g}{18g/mol}$=0.6mol,生成CO2的物质的量为$\frac{11.2L}{22.4L/mol}$=0.5mol,则烷烃分子中C原子数目为$\frac{0.5mol}{0.1mol}$=5、H原子数目为$\frac{0.6mol×2}{0.1mol}$=12,故该烷烃的分子式为C5H12,
故答案为:C5H12;
(2)C5H12有正戊烷、异戊烷、新戊烷,其中正戊烷的结构式为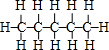 ,故答案为:
,故答案为: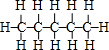 .
.
点评 本题考查有机物分子式确定,掌握燃烧法利用原子守恒确定有机物分子式,有利于基础知识的巩固.

练习册系列答案
相关题目
1.有机物的结构可用“键线式”表示,如:CH3CH=CHCH3可简写为 .有机物X的键线式为
.有机物X的键线式为 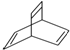 ,下列说法正确的是( )
,下列说法正确的是( )
 .有机物X的键线式为
.有机物X的键线式为  ,下列说法正确的是( )
,下列说法正确的是( )| A. | X的化学式为C8H10 | |
| B. | 有机物Y  与X互为同系物 与X互为同系物 | |
| C. | X因发生加成反应而使酸性高锰酸钾溶液褪色 | |
| D. | X与足量的H2在一定条件下反应可生成环状烃Z,Z的一氯代物有2种 |
2.下列化学用语正确的是( )
| A. | 硫化氢分子的电子式: | B. | S2-的结构示意图: | ||
| C. | HClO的结构式:H-O-Cl | D. | NH4Cl的电子式: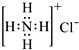 |
19.设NA为阿佛加德罗常数,下列说法错误的是( )
| A. | 在标准状况下,22.4L C5H10所含的碳原子数目为5NA | |
| B. | 常温常压下,7.8g过氧化钠含有的离子数为0.3NA | |
| C. | 18g水所含的电子数目为10NA | |
| D. | 3.2g O2、O3混合物中所含氧原子一定是0.2NA |
6.下列关于实验的叙述,正确的是( )
| A. | 滴定管的润洗是向滴定管中加入少量要盛装的溶液,边旋转边倾斜使溶液润湿全部内壁后从上口倒出 | |
| B. | 中和热的测定需要使用两个量筒分别量取酸碱溶液体积,使用两个温度计分别测定开始和终点的溶液温度 | |
| C. | 用密度为1.84g/cm3的浓硫酸配制100mL的2mol/L的稀硫酸,需要计算并称量浓硫酸的质量 | |
| D. | 用重结晶法提纯粗苯甲酸时,溶解度较小的杂质趁热过滤时留在了滤纸上,溶解度较大的杂质冷却结晶时留在了母液里 |
16.胡椒酚是植物挥发油中的一种成分.关于胡椒酚的下列说法正确的是( )
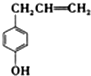

| A. | 该化合物属于芳香烃 | |
| B. | 1mol该化合物最多可与3molBr2发生反应 | |
| C. | 它的部分同分异构体能发生银镜反应 | |
| D. | 该化合物不能使酸性高锰酸钾溶液褪色 |
3.有机物分子中的原子(团)之间会相互影响,导致相同的原子(团)表现出不同的性质.下列现象不能说明上述观点的是( )
| A. | 苯酚与溴水可以直接反应,而苯与液溴反应则需要铁作催化剂 | |
| B. | 乙烯能与溴水发生加成反应,而乙烷不能与溴水发生加成反应 | |
| C. | 甲苯能使酸性KMnO4溶液褪色,而甲基环己烷不能使酸性KMnO4溶液褪色 | |
| D. | 苯酚可以与NaOH反应,而乙醇不能与NaOH反应 |
20.已知FeCl2溶液和KI溶液能发生如下反应:2FeCl3+2KI=2FeCl2+2KCl+I2,该反应属于( )
| A. | 化合反应 | B. | 置换反应 | C. | 复分解反应 | D. | 氧化还原反应 |
1.能源问题是当今世界上困扰人类发展的重大问题之一,而太阳能资源却非常丰富,开发和利用太阳能将大大缓解能源供需矛盾.下列不说法正确的是( )
| A. | 太阳能发电技术是将化学能转化为电能 | |
| B. | 集热技术是将太阳能转化为热能 | |
| C. | 光-热转化是目前最成熟、成本最低廉、应用最广泛的利用太阳能形式 | |
| D. | 化石燃料蕴藏的能量来自远古时期生物体吸收利用的太阳能 |