题目内容
按图所示实验过程填空:
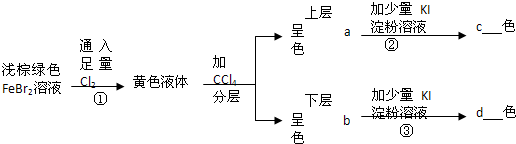
(1)写出上述反应的离子方程式:
① ② ③
(2)填空:
a b c d .

(1)写出上述反应的离子方程式:
①
(2)填空:
a
考点:物质分离和提纯的方法和基本操作综合应用,无机物的推断
专题:元素及其化合物
分析:溴化亚铁中通足量氯气,溴离子和亚铁离子均被氧化,反应的离子方程式为:3Cl2+2Fe2++4Br-=6Cl-+2Fe3++2Br2;
溴易溶于四氯化碳,由于四氯化碳密度比水大,故溴的四氯化碳在下层,呈橙红色,含铁离子的水溶液在上层,呈棕黄色,上层溶液中加入碘化钾淀粉溶液,铁离子把碘离子氧化成单质碘,反应的离子方程式为:Fe3++2I-=I2+Fe2+,碘遇淀粉变蓝色;溴的四氯化碳加入碘化钾淀粉,溴把碘离子置换出来,反应的离子方程式为:Br2+2I-=I2+2Br-,碘在四氯化碳中呈紫红色,据此分析填空.
溴易溶于四氯化碳,由于四氯化碳密度比水大,故溴的四氯化碳在下层,呈橙红色,含铁离子的水溶液在上层,呈棕黄色,上层溶液中加入碘化钾淀粉溶液,铁离子把碘离子氧化成单质碘,反应的离子方程式为:Fe3++2I-=I2+Fe2+,碘遇淀粉变蓝色;溴的四氯化碳加入碘化钾淀粉,溴把碘离子置换出来,反应的离子方程式为:Br2+2I-=I2+2Br-,碘在四氯化碳中呈紫红色,据此分析填空.
解答:
解:溴化亚铁中通足量氯气,溴离子和亚铁离子均被氧化,故①反应的离子方程式为:3Cl2+2Fe2++4Br-=6Cl-+2Fe3++2Br2;
溴易溶于四氯化碳,由于四氯化碳密度比水大,故溴的四氯化碳在下层,即b中颜色呈橙红色,含铁离子的水溶液在上层,即a中颜色呈棕黄色,上层溶液中加入碘化钾淀粉溶液,铁离子把碘离子氧化成单质碘,故②中反应的离子方程式为:Fe3++2I-=I2+Fe2+,碘遇淀粉变蓝色,故c中颜色为蓝色;溴的四氯化碳加入碘化钾淀粉,溴把碘离子置换出来,故③中反应的离子方程式为:Br2+2I-=I2+2Br-,碘在四氯化碳中呈紫红色,故d中颜色呈紫红色.
故答案为:(1)3Cl2+2Fe2++4Br-=6Cl-+2Fe3++2Br2;Fe3++2I-=I2+Fe2+;Br2+2I-=I2+2Br-;
(2)棕黄;橙红;蓝;紫红.
溴易溶于四氯化碳,由于四氯化碳密度比水大,故溴的四氯化碳在下层,即b中颜色呈橙红色,含铁离子的水溶液在上层,即a中颜色呈棕黄色,上层溶液中加入碘化钾淀粉溶液,铁离子把碘离子氧化成单质碘,故②中反应的离子方程式为:Fe3++2I-=I2+Fe2+,碘遇淀粉变蓝色,故c中颜色为蓝色;溴的四氯化碳加入碘化钾淀粉,溴把碘离子置换出来,故③中反应的离子方程式为:Br2+2I-=I2+2Br-,碘在四氯化碳中呈紫红色,故d中颜色呈紫红色.
故答案为:(1)3Cl2+2Fe2++4Br-=6Cl-+2Fe3++2Br2;Fe3++2I-=I2+Fe2+;Br2+2I-=I2+2Br-;
(2)棕黄;橙红;蓝;紫红.
点评:本题考查了氯溴碘氧化性顺序和铁离子的氧化性,中等难度,明确离子的还原性顺序或卤素单质的氧化性顺序是解题关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
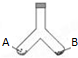 如图所示是一密闭容器,已知A端盛2.3g金属钠,B端盛有xgHgO,当同时加热容器的两侧支管时,钠着火燃烧,冷却后测得容器中空气成分并未发生变化,求x的值.(Hg的相对原子质量是200.6)
如图所示是一密闭容器,已知A端盛2.3g金属钠,B端盛有xgHgO,当同时加热容器的两侧支管时,钠着火燃烧,冷却后测得容器中空气成分并未发生变化,求x的值.(Hg的相对原子质量是200.6)