题目内容
5.钙元素对人类的生产、生活具有重要意义.(1)儿童缺钙可能会导致佝偻病(填“贫血”或“佝偻病”).
(2)次氯酸钙[Ca(ClO)2]是重要的消毒剂,次氯酸钙中氯元素的化合价是+1.
(3)氧化钙能与水反应,化学方程式为CaO+H2O=Ca(OH)2,该反应可用于制取熟石灰(加热食品、吸收水分).
分析 (1)根据钙元素与人体健康之间的关系分析;
(2)根据化合价原则,求出元素的化合价;
(3)根据氧化钙能与水反应分析回答.
解答 解:(1)钙主要存在于骨胳和牙齿中,使骨和牙齿具有坚硬的结构支架,儿童缺钙可能会导致佝偻病,故答案为:佝偻病;
(2)据在化合物中正负化合价代数和为零,钙元素显+2,氧元素显-2,设氯元素的化合价是x,可知次氯酸钙Ca(ClO)2中氯元素的化合价:(+2)+2x+(-2)×2=0,则x=+1,故答案为:+1;
(3)氧化钙能与水反应,化学方程式为CaO+H2O=Ca(OH)2,该反应可用于制取熟石灰,故答案为:CaO+H2O=Ca(OH)2;制取熟石灰.
点评 本题难度不大,考查利用化合价的原则计算指定元素的化合价、方程式的书写等能力,注意基础知识的积累.

练习册系列答案
相关题目
16.可用于鉴别氧化铜、铁粉、炭粉、二氧化锰四种黑色粉末(必要时可加热)的试剂是( )
| A. | 水 | B. | 氢氧化钠溶液 | C. | 浓盐酸 | D. | 氯化铁溶液 |
13.可用作磁性材料的物质是( )
| A. | FeO | B. | Fe2O3 | C. | Fe3O4 | D. | FeS |
20.在下列化学方程式中,不能够用离子方程式Ba2++SO42-═BaSO4↓表示的是( )
| A. | BaCl2+K2SO4═BaSO4↓+2KCl | B. | BaCO3+H2SO4═BaSO4↓+CO2↑+H2O | ||
| C. | Ba(NO3)2+H2SO4═BaSO4↓+2HNO3 | D. | Ba(OH)2+2KHSO4═BaSO4↓+K2SO4+2H2O |
10.下列对于Na2O、Na2O2的比较正确的一项是( )
| A. | Na2O、Na2O2都是钠的氧化物,都是碱性氧化物 | |
| B. | Na2O、Na2O2都是易溶于水(与水反应)的白色固体 | |
| C. | Na2O2在和CO2的反应中既是氧化剂又是还原剂 | |
| D. | Na2O2与水反应时,1mol Na2O2转移2 mol电子 |
17.利用如图所示装置进行下列实验,将X溶液逐滴加入固体Y中,装置B的试管中的现象不
正确的是( )
正确的是( )
| 选项 | X溶液 | 固体Y | Z溶液 | 现象 |  |
| A | 稀硫酸 | 亚硫酸氢钠 | 品红试剂 | 品红褪色 | |
| B | 浓氨水 | CaO | 紫色石蕊试液 | 溶液变红 | |
| C | 盐酸 | 石灰石 | 硅酸钠溶液 | 出现白色沉淀 | |
| D | 双氧水 | MnO2 | 氢硫酸溶液 | 产生浑浊 |
| A. | A | B. | B | C. | C | D. | D |
15.某离子反应中涉及H2O、ClO?、NH4+、H+、N2、Cl-六种微粒.其中N2的物质的量随时间变化的曲线如图所示.下列判断正确的是( )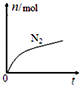

| A. | 该反应的还原剂是Cl- | |
| B. | 消耗1 mol还原剂,转移6 mol电子 | |
| C. | 氧化剂与还原剂的物质的量之比为2:3 | |
| D. | 反应后溶液的酸性明显增强 |