题目内容
 CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径.
CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径.(1)下列措施中,有利于降低大气中的CO2、SO2、NOx浓度的有
a.减少化石燃料的使用,开发新能源
b.使用无氟冰箱,减少氟里昂排放
c.多步行或乘公交车,少用专车或私家车
d.将工业废气用碱液吸收后再排放
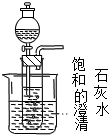
(2)有学者设想以如图所示装置用电化学原理将CO2、SO2 转化为重要化工原料.
若A为CO2,B为H2,C为CH3OH,则通入CO2的一极为
(3)①在研究氮的氧化物的转化时,某小组查阅到以下数据:17℃、1.01×105Pa时,2NO2(g)?N2O4(g)△H<0的平衡常数 K=13.3,则该条件下密闭容器中N2O4 和NO2的混合气体达到平衡时,若 c (NO2)=0.0300mol?L-1,c (N2O4)=
②若改变上述体系的某个条件,达到新的平衡后,测得混合气体中 c (NO2)=0.04mol?L-1,c (N2O4)=0.007mol?L-1,则改变的条件为
(4)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代作为公交车的燃料.写出用合成气(CO和H2)生产甲醇的化学方程式
| 3 |
| 2 |
考点:常见的生活环境的污染及治理,用盖斯定律进行有关反应热的计算,化学电源新型电池,化学平衡的影响因素
专题:化学反应中的能量变化,化学平衡专题,电化学专题
分析:(1)a、化石燃料的废气中均含有CO2、SO2、NOx等气体;
b、氟利昂的排放会破坏臭氧层,故b错误;
c、汽车燃烧的废气中均含有CO2、SO2、NOx等气体;
d、工业废气中的CO2、SO2、NOx等气体均是酸性气体,可以被碱液吸收;
(2)燃料电池的工作原理,正极上是CO2发生得电子的还原反应;负极上二氧化硫失电子发生氧化反应;
(3)①根据平衡常数与物质浓度之间的关系式计算;
②根据其平衡常数判断;
(4)一氧化碳和氢气反应生成甲醇,该反应属于化合反应,原子利用率高;根据甲醇的燃烧热书写其热化学反应方程式;
b、氟利昂的排放会破坏臭氧层,故b错误;
c、汽车燃烧的废气中均含有CO2、SO2、NOx等气体;
d、工业废气中的CO2、SO2、NOx等气体均是酸性气体,可以被碱液吸收;
(2)燃料电池的工作原理,正极上是CO2发生得电子的还原反应;负极上二氧化硫失电子发生氧化反应;
(3)①根据平衡常数与物质浓度之间的关系式计算;
②根据其平衡常数判断;
(4)一氧化碳和氢气反应生成甲醇,该反应属于化合反应,原子利用率高;根据甲醇的燃烧热书写其热化学反应方程式;
解答:
解:(1)a、化石燃料的废气中均含有CO2、SO2、NOx等气体,减少化石燃料的使用,开发新能源,可以降低大气中的CO2、SO2、NOx浓度,故a正确;
b、使用无氟冰箱,减少氟里昂排放,可以减少臭氧层的破坏,故b错误;
c、汽车燃烧的废气中均含有CO2、SO2、NOx等气体,多步行或乘公交车,少用专车或私家车,可以降低大气中的CO2、SO2、NOx浓度,故c正确;
d、工业废气中的CO2、SO2、NOx等气体均是酸性气体,可以和碱液反应生成盐,被碱液吸收后再排放,可以降低大气中的CO2、SO2、NOx浓度,故d正确.
故选acd;
(2)燃料电池的工作时,若A为CO2,B为H2,C为CH3OH,则正极上是CO2发生得电子得还原反应,即CO2+6H++6e-=CH3OH+H2O,
若A为SO2,B为O2,C为H2SO4时,负极上二氧化硫失电子和水反应生成硫酸,电极反应式为:SO2+2H2O-2e-=4H++SO42-,
故答案为:正;SO2+2H2O-2e-=4H++SO42-;
(3)①c(N2O4)=Kc2(NO2)=13.3×(0.0300)2mol/L=0.012mol/L,
故答案为:0.012mol/L;
②再次平衡时平衡常数K′=
=4.375<13.3,平衡常数减小,则反应向逆反应方向移动,改变条件是升高温度,
故答案为:升温;
(4)根据题意由CO和H2生产甲醇解题,得CO+2H2=CH3OH;根据液态甲醇燃烧生成二氧化碳和水蒸气,化学方程式为:2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g),根据盖斯定律得:①CO+2H2=CH3OH△H1=+131.9kJ?mol-1②2H2(g)+CO(g)+
O2(g)=CO2(g)+2H2O(g)△H2=-594.1kJ?mol-1
③2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H3
③=2×(②-①)△H3=2×(△H2-△H1)=-1452kJ?mol-1
故答案为:CO+2H2=CH3OH;2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H=-1452kJ?mol-1;
b、使用无氟冰箱,减少氟里昂排放,可以减少臭氧层的破坏,故b错误;
c、汽车燃烧的废气中均含有CO2、SO2、NOx等气体,多步行或乘公交车,少用专车或私家车,可以降低大气中的CO2、SO2、NOx浓度,故c正确;
d、工业废气中的CO2、SO2、NOx等气体均是酸性气体,可以和碱液反应生成盐,被碱液吸收后再排放,可以降低大气中的CO2、SO2、NOx浓度,故d正确.
故选acd;
(2)燃料电池的工作时,若A为CO2,B为H2,C为CH3OH,则正极上是CO2发生得电子得还原反应,即CO2+6H++6e-=CH3OH+H2O,
若A为SO2,B为O2,C为H2SO4时,负极上二氧化硫失电子和水反应生成硫酸,电极反应式为:SO2+2H2O-2e-=4H++SO42-,
故答案为:正;SO2+2H2O-2e-=4H++SO42-;
(3)①c(N2O4)=Kc2(NO2)=13.3×(0.0300)2mol/L=0.012mol/L,
故答案为:0.012mol/L;
②再次平衡时平衡常数K′=
| 0.007 |
| 0.04×0.04 |
故答案为:升温;
(4)根据题意由CO和H2生产甲醇解题,得CO+2H2=CH3OH;根据液态甲醇燃烧生成二氧化碳和水蒸气,化学方程式为:2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g),根据盖斯定律得:①CO+2H2=CH3OH△H1=+131.9kJ?mol-1②2H2(g)+CO(g)+
| 3 |
| 2 |
③2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H3
③=2×(②-①)△H3=2×(△H2-△H1)=-1452kJ?mol-1
故答案为:CO+2H2=CH3OH;2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H=-1452kJ?mol-1;
点评:本题考查了原电池原理、化学平衡的有关计算、盖斯定律等知识点,难点是化学平衡的有关计算,此点也是考试热点,题目难度中等.

练习册系列答案
相关题目
下列反应既是化合反应,又是氧化反应的是( )
A、2CO+O2
| ||||
| B、CaO+H2O=Ca(OH)2 | ||||
C、C+H2O
| ||||
| D、CO2+Ca(OH)2=CaCO3↓+H2O |
在光照条件下,将a mol甲烷与足量Cl2反应,测知四种产物的物质的量比依次2:1:1:2,则耗Cl2的物质的量为( )
| A、a mol |
| B、1.25a mol |
| C、2.5a mol |
| D、4a mol |
下列图象中,横坐标为溶液中加入反应物的物质的量,纵坐标为沉淀物的量,则相应的图象序号与(1)--(5)对应的顺序正确的是( )


| 溶液 | 加入物质 |
| (1)氯化铝溶液 | 加入过量氨水 |
| (2)饱和石灰水 | 通过量CO2气体 |
| (3)MgCl2、AlCl3的混合液 | 逐滴加入NaOH溶液至过量 |
| (4)含少量NaOH的NaAlO2溶液 | 逐滴加入稀盐酸 |
| (5)含少量HCl的AlCl3溶液 | 逐滴加入过量的氨水 |
| A、③①②④⑤ |
| B、③②①⑤④ |
| C、①③②⑤④ |
| D、①③②④⑤ |
某无色溶液中可能含有I-、K+、Cu2+、SO32-(还原性:SO32->I-),向该溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液组成的判断正确的是( )
①肯定不含I-; ②肯定不含Cu2+; ③肯定含有SO32-; ④可能含有I-.
①肯定不含I-; ②肯定不含Cu2+; ③肯定含有SO32-; ④可能含有I-.
| A、①③ | B、①②③ |
| C、②③④ | D、①② |
用NA表示阿伏伽德罗常数的值,下列说法不正确的是( )
| A、常温下,1mol甲烷含有的氢原子数为4NA |
| B、2g氦气所含有原子数为0.5NA |
| C、0.1mol/L的硫酸铝溶液中含SO42-数为0.3NA |
| D、18g水所含质子数为10NA |
合成氨反应:N2(g)+3H2(g)?2NH3(g)△H,若该反应在一定条件下能自发,则有关该反应的△H、△S判断正确的是( )
| A、△H<0△S<0 |
| B、△H<0△S>0 |
| C、△H>0△S<0 |
| D、△H>0△S>0 |