��Ŀ����
 �ס��ҡ���������ԭ������������20��Ԫ����ɵ����ʣ����ʻ�����Ҵ�������ת����ϵ����+�ҡ���+�������λش��������⣺
�ס��ҡ���������ԭ������������20��Ԫ����ɵ����ʣ����ʻ�����Ҵ�������ת����ϵ����+�ҡ���+�������λش��������⣺��1��ת����ϵ�����漰�ķ�ӦΪ��������ԭ��Ӧ������Ϊ����10���ӷ���ʱ��
������Ϊ��ȼ�����壬���ӵĿռ乹��Ϊֱ���νṹ����֪���ȼ��ag������ʱ����1mol������̼��Һ̬ˮ�����ų�����bkJ�������ȼ�յ��Ȼ�ѧ����ʽΪ
����������7��Ԫ�غ�17��Ԫ����ɵĻ������������ģ����ͼ��ʾ��������Ư���ԣ������17��Ԫ�صĻ��ϼ���
��2��ת����ϵ�����漰�ķ�ӦΪ������ԭ��Ӧ������Ϊ����10���ӷ���ʱ��
���������ڷ�����ߡ�DZͧ�ȳ��õĹ�������д��������Ӧ�Ļ�ѧ����ʽ
�������Ͷ����ǿ�ȼ�����壬���б��ǹ�ҵ���������л�ԭ����д�����淴Ӧ��+�ҡ�+��+���Ļ�ѧƽ�ⳣ���ı���ʽ
����������N��0Ԫ����ɵ���̬���ʣ��ʺ���ɫ����3.36gFe�ӵ�һ��������Һ�У��ռ���1.12L���嶡��������Ϊ��״��������Fe�����Һ��Ӧ�����ӷ���ʽ��
���㣺������ƶ�
ר�⣺�ƶ���
��������1��ת����ϵ�����漰�ķ�ӦΪ��������ԭ��Ӧ������Ϊ����10���ӷ��ӣ�
������Ϊ��ȼ�����壬���ӵĿռ乹��Ϊֱ���νṹ�����ΪC2H2����Ϊ����10���ӷ��ӣ��Ҹ÷�ӦΪ��������ԭ��Ӧ����ΪH2O����+�ҡ���+���ķ�Ӧ����ʽΪCaC2+2H2O=Ca��OH��2+C2H2�������ȼ��
mol��Ȳ����ʱ����1mol������̼��Һ̬ˮ�����ų�����bkJ��ag��Ȳ�����ʵ���Ϊ
=
mol����1mol��Ȳ��ȫȼ�շų�����Ϊ
kJ���ݴ���д���Ȼ�ѧ����ʽ��
����������7��Ԫ�غ�17��Ԫ����ɵĻ�����NCl3������ˮ��������Ư���ԣ����Ա���HClO����ΪNH3�����+�ҡ���+���ķ�Ӧ����ʽΪNCl3+3H2O=3HClO+NH3��������Ԫ�ػ��ϼ۵Ĵ�����Ϊ0ȷ��ClԪ�ػ��ϼۣ�
��2��ת����ϵ�����漰�ķ�ӦΪ������ԭ��Ӧ������Ϊ����10���ӷ��ӣ�
���������ڷ�����ߡ�DZͧ�ȳ��õĹ������������Na2O2������H2O��
�������Ͷ����ǿ�ȼ�����壬���б��ǹ�ҵ���������л�ԭ���������CO���÷�ӦΪC��ˮ�����ķ�Ӧ����Ӧ����ʽΪC+H2O?CO+H2��
����������N��0Ԫ����ɵ���̬���ʣ��ʺ���ɫ�������NO2��n��Fe��=
=0.06mol������������ˮ��Ӧ����HNO3��NO����Ϊ���壬����NO������HNO3��n��NO��=
=0.05mol���ݴ���д���ӷ���ʽ��
������Ϊ��ȼ�����壬���ӵĿռ乹��Ϊֱ���νṹ�����ΪC2H2����Ϊ����10���ӷ��ӣ��Ҹ÷�ӦΪ��������ԭ��Ӧ����ΪH2O����+�ҡ���+���ķ�Ӧ����ʽΪCaC2+2H2O=Ca��OH��2+C2H2�������ȼ��
| a |
| 26 |
| ag |
| 26g/mol |
| a |
| 26 |
| 26b |
| a |
����������7��Ԫ�غ�17��Ԫ����ɵĻ�����NCl3������ˮ��������Ư���ԣ����Ա���HClO����ΪNH3�����+�ҡ���+���ķ�Ӧ����ʽΪNCl3+3H2O=3HClO+NH3��������Ԫ�ػ��ϼ۵Ĵ�����Ϊ0ȷ��ClԪ�ػ��ϼۣ�
��2��ת����ϵ�����漰�ķ�ӦΪ������ԭ��Ӧ������Ϊ����10���ӷ��ӣ�
���������ڷ�����ߡ�DZͧ�ȳ��õĹ������������Na2O2������H2O��
�������Ͷ����ǿ�ȼ�����壬���б��ǹ�ҵ���������л�ԭ���������CO���÷�ӦΪC��ˮ�����ķ�Ӧ����Ӧ����ʽΪC+H2O?CO+H2��
����������N��0Ԫ����ɵ���̬���ʣ��ʺ���ɫ�������NO2��n��Fe��=
| 3.36g |
| 56g/mol |
| 1.12L |
| 22.4L/mol |
���
�⣺�ס��ҡ���������ԭ������������20��Ԫ����ɵ����ʣ����ʻ��������ת����ϵ����+��һ��+����
��1��ת����ϵ�����漰�ķ�ӦΪ��������ԭ��Ӧ������Ϊˮʱ��
������Ϊ��ȼ�����壬���ӵĿռ乹��Ϊֱ���νṹ�����ΪC2H2����Ϊ����10���ӷ��ӣ��Ҹ÷�ӦΪ��������ԭ��Ӧ����ΪH2O����+�ҡ���+���ķ�Ӧ����ʽΪCaC2+2H2O=Ca��OH��2+C2H2�������ȼ��
mol��Ȳ����ʱ����1mol������̼��Һ̬ˮ�����ų�����bkJ��ag��Ȳ�����ʵ���Ϊ
=
mol����1mol��Ȳ��ȫȼ�շų�����Ϊ
kJ�����Ȼ�ѧ����ʽΪC2H2��g��+
O2��g��=2CO2��g��+H2O��l����H=-
kJ/mol��
�ʴ�Ϊ��C2H2��g��+
O2��g��=2CO2��g��+H2O��l����H=-
kJ/mol��
����������N��ClԪ����ɵĻ�����ɼ������ģ�Ϳ�֪���ϴ���ΪClԭ�ӡ���С��ΪNԭ�ӣ���ΪNCl3������ˮ�ⷴӦ������Ư���ԣ����ΪHClO����ΪNH3����NCl3��N���ָ��ۡ�ClΪ���ۣ���NCl3��NΪ-3�ۡ�ClΪ+1�ۣ�
�ʴ�Ϊ��+1��
��2��ת����ϵ�����漰�ķ�ӦΪ������ԭ��Ӧ������Ϊˮʱ��
���������ڷ�����ߡ�DZͧ�ȳ��õĹ����������ΪNa2O2����ˮ��Ӧ����������������������Ӧ����ʽΪ��2Na2O2+2H2O=4NaOH+O2����
�ʴ�Ϊ��2Na2O2+2H2O=4NaOH+O2����
�������Ͷ����ǿ�ȼ�����壬���б��ǹ�ҵ���������л�ԭ�������ΪCO���ʼ�Ϊ̼����Ϊ�������÷�Ӧ����ʽΪ��C+H2O?CO+H2����ѧƽ�ⳣ��K=
��
�ʴ�Ϊ��K=
��
����������N��OԪ����ɵ���̬���ʣ��ʺ���ɫ�����ΪNO2����ˮ��Ӧ����������NO��Fe�ӵ�һ��������Һ�����嶡�����Ϊ���ᡢ��ΪNO������Һ��Fe3+��Fe2+�����ʵ����ֱ�Ϊxmol��ymol����
���x=0.03��y=0.03��
�ʷ�Ӧ���ӷ���ʽΪ��6Fe+5NO3-+2OH+=3Fe3++3Fe2++5NO��+10H2O��
�ʴ�Ϊ��6Fe+5NO3-+2OH+=3Fe3++3Fe2++5NO��+10H2O��
��1��ת����ϵ�����漰�ķ�ӦΪ��������ԭ��Ӧ������Ϊˮʱ��
������Ϊ��ȼ�����壬���ӵĿռ乹��Ϊֱ���νṹ�����ΪC2H2����Ϊ����10���ӷ��ӣ��Ҹ÷�ӦΪ��������ԭ��Ӧ����ΪH2O����+�ҡ���+���ķ�Ӧ����ʽΪCaC2+2H2O=Ca��OH��2+C2H2�������ȼ��
| a |
| 26 |
| ag |
| 26g/mol |
| a |
| 26 |
| 26b |
| a |
| 5 |
| 2 |
| 26b |
| a |
�ʴ�Ϊ��C2H2��g��+
| 5 |
| 2 |
| 26b |
| a |
����������N��ClԪ����ɵĻ�����ɼ������ģ�Ϳ�֪���ϴ���ΪClԭ�ӡ���С��ΪNԭ�ӣ���ΪNCl3������ˮ�ⷴӦ������Ư���ԣ����ΪHClO����ΪNH3����NCl3��N���ָ��ۡ�ClΪ���ۣ���NCl3��NΪ-3�ۡ�ClΪ+1�ۣ�
�ʴ�Ϊ��+1��
��2��ת����ϵ�����漰�ķ�ӦΪ������ԭ��Ӧ������Ϊˮʱ��
���������ڷ�����ߡ�DZͧ�ȳ��õĹ����������ΪNa2O2����ˮ��Ӧ����������������������Ӧ����ʽΪ��2Na2O2+2H2O=4NaOH+O2����
�ʴ�Ϊ��2Na2O2+2H2O=4NaOH+O2����
�������Ͷ����ǿ�ȼ�����壬���б��ǹ�ҵ���������л�ԭ�������ΪCO���ʼ�Ϊ̼����Ϊ�������÷�Ӧ����ʽΪ��C+H2O?CO+H2����ѧƽ�ⳣ��K=
| c(CO)��c(H2) |
| c(H2O) |
�ʴ�Ϊ��K=
| c(CO)��c(H2) |
| c(H2O) |
����������N��OԪ����ɵ���̬���ʣ��ʺ���ɫ�����ΪNO2����ˮ��Ӧ����������NO��Fe�ӵ�һ��������Һ�����嶡�����Ϊ���ᡢ��ΪNO������Һ��Fe3+��Fe2+�����ʵ����ֱ�Ϊxmol��ymol����
|
�ʷ�Ӧ���ӷ���ʽΪ��6Fe+5NO3-+2OH+=3Fe3++3Fe2++5NO��+10H2O��
�ʴ�Ϊ��6Fe+5NO3-+2OH+=3Fe3++3Fe2++5NO��+10H2O��
���������⿼�������ƶϡ����ӷ���ʽ����д����ѧƽ�ⳣ�����塢�Ȼ�ѧ����ʽ��֪ʶ�㣬�ۺ��Խ�ǿ���ѵ��ǣ�2���������ӷ���ʽ����д��Ҫ����ת�Ƶ����غ�ȷ����Ԫ�ؼ�̬���������֮�ȣ���Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 һ����ʦȨ����ҵ��ϵ�д�
һ����ʦȨ����ҵ��ϵ�д�
�����Ŀ
���и����ʣ����յ��ʡ�������������࣬������ȷ���ǣ�������
| A�������ɱ���ˮ���� |
| B��������������С�մ� |
| C����Һ�ȡ���ˮ��Ư�۾� |
| D�����������졢���� |
���и������ʵľ����У���ѧ��������ͬ����������Ҳ��ͬ���ǣ�������
| A��SO2��SiO2 |
| B��HCl��AlCl3 |
| C��NaCl��NaOH |
| D��CCl4��KCl |
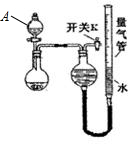



 Ҳ����CH3CHO�������Ʒ�Ӧ�ٵķ�Ӧ�������л���÷�Ӧ��ѧ����ʽΪ
Ҳ����CH3CHO�������Ʒ�Ӧ�ٵķ�Ӧ�������л���÷�Ӧ��ѧ����ʽΪ ����ͼװ�ý�������ʵ�飬�ܵó���Ӧʵ����۵��ǣ�������
����ͼװ�ý�������ʵ�飬�ܵó���Ӧʵ����۵��ǣ������� ����2013���������ҹ��ж����������������Χ����ʱ������������������ŷŵĵ������úȼ�ղ����Ķ��������ǵ������������ġ�������ס���
����2013���������ҹ��ж����������������Χ����ʱ������������������ŷŵĵ������úȼ�ղ����Ķ��������ǵ������������ġ�������ס���