题目内容
13.除去Na2CO3粉末中混入的NaHCO3杂质用加热方法,化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.分析 碳酸氢钠加热分解生成碳酸钠,则加热可除杂,以此来解答.
解答 解:除去Na2CO3粉末中混入的NaHCO3杂质用加热方法,化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,
故答案为:加热;2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
点评 本题考查混合物的分离提纯,为高频考点,把握物质的性质、发生的反应、混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案
相关题目
1.下列说法中,正确的是( )
| A. | 分子间作用力越大,分子越稳定 | |
| B. | 气态氢化物共价键越强,热稳定性越高 | |
| C. | 冰融化时水分子中共价键发生断裂 | |
| D. | 氢键是化学键的一种类型 |
8.反应Cu2++Zn=Cu+Zn2+可在溶液中进行完全,由该反应可判断Cu2+的氧化性强于( )
| A. | Zn | B. | Cu | C. | Zn2+ | D. | Cu+ |
18.下列原子中可以形成R+离子的是( )
| A. | 核电荷数为13 | B. | 质子数为17 | ||
| C. | M层比L层少6 | D. | 质量数为23,中子数为12 |
5.下列过程中,既有离子键被破坏,又有共价键被破坏的是( )
| A. | 溴蒸汽被木炭吸附 | B. | 烧碱熔化 | ||
| C. | 碳酸钙高温分解 | D. | HCl溶于水 |
2.下列装置或操作(有的夹持装置已省略)正确且能达到目的是( )
| A. | 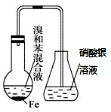 验证苯和液溴在催化剂作用下发生取代反应 | |
| B. | 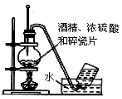 实验室制备并收集乙烯 | |
| C. | 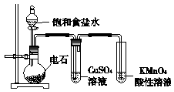 制备乙炔并检验其性质 | |
| D. | 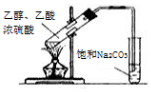 乙醇与乙酸反应制备乙酸乙酯 |
3.下列关于物质的性质与应用具有对应关系的是( )
| A. | 氧化铁能与酸反应,可用于制作红色涂料 | |
| B. | NaHCO3能与碱反应,可用作焙制糕点的膨松剂 | |
| C. | 铜的金属活动性比铁弱,可用铜罐代替铁罐贮运浓硝酸 | |
| D. | 氢氧化铝具有弱性,可用于制胃酸中和剂 |
 ;
; ;
;