题目内容
下列叙述正确的是( )
| A、32g O2含有氧原子数为6.02×1023 |
| B、18g H2O在标准状况下的体积是22.4L |
| C、将80g NaOH溶于1L水中,所得溶液中NaOH的物质的量浓度为2mol/L |
| D、常温常压下,14g N2含有分子数为3.01×1023 |
考点:物质的量的相关计算
专题:计算题
分析:根据n=
=
=
结合物质的构成以及存在的条件、聚集状态解答该题.
| m |
| M |
| N |
| NA |
| V |
| Vm |
解答:
解:A.n( O2)=
=1mol,n(O)=2mol,N(O)=1.204×1024,故A错误;
B.标准状况下水为液体,故B错误;
C.1L水的体积不等于溶液的体积,故C错误;
D.n(N2)=
=0.5mol,分子数为3.01×1023,故D正确.
故选D.
| 32g |
| 32g/mol |
B.标准状况下水为液体,故B错误;
C.1L水的体积不等于溶液的体积,故C错误;
D.n(N2)=
| 14g |
| 28g/mol |
故选D.
点评:本题考查物质的量的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握相关计算公式的运用,难度不大,注意物质存在的条件和状态.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列举措不符合“节能减排”要求的是( )
| A、在西部和沿海地区兴建风力发电站,解决能源问题 |
| B、推广与发展小排量汽车和电动、混合动力汽车 |
| C、大力开发丰富的煤炭资源,减少对石油的依赖 |
| D、回收废弃饮料包装纸,制作成公园内的休闲长椅 |
设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、常温常压下,NA个CO2分子的体积为22.4L |
| B、常温常压下,1mol氦气含有的核外电子数为4 NA |
| C、12.4g白磷(P4)中含有的磷原子数为0.4 NA |
| D、标准状况下,22.4L氧气所含质子数是8NA |
下列过程中共价键被破坏的是( )
| A、碘升华 |
| B、食盐熔化 |
| C、水电解生成氢气和氧气 |
| D、水结成冰 |
下列变化不属于氧化还原反应的是( )
| A、2HClO═2HCl+O2↑ | ||||
| B、2Na2O2+2CO2═2Na2CO3+O2 | ||||
| C、4Fe(OH)2+O2+2H2O═4Fe(OH)3 | ||||
D、2NaHCO3
|
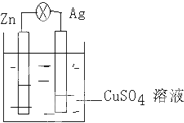 在银锌原电池中,以硫酸铜为电解质溶液,
在银锌原电池中,以硫酸铜为电解质溶液,