题目内容
12.硫酸厂有一辆存放过浓硫酸的铁槽车,某新工人违反操作规程,边吸烟边用水冲洗,结果发生了爆炸事故.下列所述引起爆炸的原因,正确的是( )| A. | 硫酸遇明火发热爆炸 | |
| B. | 浓硫酸遇水发热爆炸 | |
| C. | 铁与水反应产生氢气,氢气接触空气后遇明火爆炸 | |
| D. | 稀释后的硫酸与铁反应产生氢气接触明火爆炸 |
分析 铁槽车上的铁与稀释后的硫酸反应产生氢气,混有了空气,遇到明火,发生了爆炸.
解答 解:A、浓硫酸以吸收空气中的水蒸气,但不会遇空气爆炸,故A错误;
B、稀释浓硫酸会放出热量,放出大量的热可使水沸腾,不至于发生爆炸,故B错误;
C、常温下铁与水不会发生反应产生氢气,故C错误;
D、浓硫酸稀释后变成稀硫酸,与铁反应生成氢气,遇到明火发生了爆炸,故D正确;
故选D.
点评 本题主要考查了硫酸的性质及爆炸的相关知识,渗透了生活与化学息息相关的理念,提醒同学们要把生活中的一些现象与相应的化学知识联系起来,学会用化学知识去分析和解答问题,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.常温下,下列各组离子一定能大量共存的是( )
| A. | c(H+)=10-4mol•L-1的溶液中:NH4+、K+、SO42-、NO3- | |
| B. | 无色溶液中:Na+、Cu2+、Cl-、NO3- | |
| C. | 0.1 mol•L-1AgNO3 溶液:H+、K+、SO42-、I- | |
| D. | 饱和氯水中:Cl-、Na+、NO3-、SO32- |
20.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1mol乙醚中含有的C-O键的数目为2NA | |
| B. | 标准状况下,44.8CHCl3中含有分子的数目为2NA | |
| C. | 1 mol-CH3中所含的电子总数为10 NA | |
| D. | 向FeI2溶液中通入适量Cl2,当有2 mol Fe2+被氧化时,消耗Cl2的分子数为NA |
17.某元素基态原子失去3个电子后,3d轨道半充满,其原子序数为( )
| A. | 24 | B. | 25 | C. | 26 | D. | 27 |
4.下列说法正确的是( )
| A. | 往某溶液中加入稀NaOH溶液,无刺激性气味的气体产生,说明该溶液一定不含NH4+ | |
| B. | 用加热的方法可以除去混在NaCl固体中的NH4Cl,说明NH4Cl会升华 | |
| C. | SO2气体和Cl2均能使品红溶液褪色,说明两者均有强氧化性 | |
| D. | 浓硫酸可用来干燥H2、Cl2、SO2等气体,说明浓硫酸具有吸水性 |
1.某溶液既能溶解Al(OH)3,又能溶解H2SiO3的溶液,在该溶液中可以大量共存的离子组是( )
| A. | K+、Na+、HCO${\;}_{3}^{-}$、NO3- | B. | Na+、SO${\;}_{4}^{2-}$、Cl-、ClO- | ||
| C. | H+、Mg2+、SO${\;}_{4}^{2-}$、NO3- | D. | Ag+、K+、NO3-、Na+ |
2.设NA表示阿伏伽德罗常数,下列叙述中正确的是( )
| A. | 常温常压下,11.2L氧气中所含有的原子数为NA | |
| B. | 17g的NH3分子中含有的电子数为10NA | |
| C. | 常温常压下,48g O3含有的氧原子数为3NA | |
| D. | 标准状况下,11.2LH2O中所含有的分子数为0.5NA |
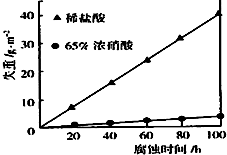 按要求回答下列问题:
按要求回答下列问题: ;
;