题目内容
11.某工厂燃料煤中硫的质量分数为0.64%,该工厂每天燃烧这种煤10吨,试计算:1)如果煤中的硫全部转化为SO2,该工厂每天产生的SO2在标准状况下的体积为多少升?
2)如果把产生的SO2全部利用收回,理论上每年(按360天计)可得到98%的浓硫酸的质量为多少吨?
分析 1)利用n=$\frac{m}{M}$=计算煤中S原子物质的量,根据反应的关系式S~SO2计算SO2的物质的量,再根据V=nVm计算;
2)根据反应的关系式SO2~H2SO4,计算生成硫酸的质量,结合质量分数计算溶液的质量.
解答 解:1)m(S)=10t×0.64%=0.064t=64000g,
n(S)=$\frac{64000g}{32g/mol}$=2000mol,
由反应的关系式S~SO2,可知:n(SO2)=n(S)=2000mol,
V(SO2)=2000mol×22.4L/mol=4.48×104L,
答:该工厂每天产生的SO2在标准状况下的体积为4.48×104L;
2)每天生成2000 mol SO2 2×104mol,则每年生成SO2 为2000mol×360=7.2×105mol,
由反应的关系式SO2~H2SO4,可知生成n(H2SO4)=7.2×105mol,
则m(H2SO4)=7.2×105mol×98g/mol
得到98%的浓硫酸(密度为1.84g/cm3)的质量为:$\frac{7.2×1{0}^{5}mol×98g/mol}{98%}$=7.2×107g=72t,
答:理论每年得到98%的浓硫酸的质量为72t.
点评 本题考查化学方程式的计算,题目难度中等,注意根据S元素守恒利用关系式计算解答,避免方程式的繁琐.

练习册系列答案
 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案
相关题目
1.升高温度,0.01mol•L-1下列溶液的pH基本不变的是( )
| A. | NaOH | B. | NaCl | C. | H2SO4 | D. | NH4Cl |
2.下列无色溶液中的离子能大量共存的是( )
| A. | K+、Na+、MnO4-、SO42- | B. | OH-、K+、HCO3-、SO32- | ||
| C. | Na+、Ba2+、Cl-、Br- | D. | Fe3+、NH4+、SCN-、NO3- |
6.在含有大量的K+、NH4+、Cl-、SO42-的溶液中还可能大量存在的离子是( )
| A. | H+ | B. | Ag+ | C. | OH- | D. | Ba2+ |
16.下列各组离子,在所给的条件下,一定能够大量共存的是( )
| A. | 在pH=0的溶液中:Fe2+、Mg2+、CO32-、NO3- | |
| B. | 在由水电离出的c(H+)=1×10-12mol/L的溶液中:HCO3-、Al3+、NH4+、ClO- | |
| C. | 在滴加酸碱指示剂酚酞试液后呈现红色的溶液中:Na+、Cl-、AlO2-、CO32- | |
| D. | 在AlCl3溶液中:K+、NO3-、OH-、Na+. |
3.α,β,γ和δ4种生育三烯酚(见图)是构成维生素E的主要物质,下列叙述中不正确的是( )
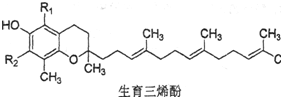

| α β γ δ | |
| R1 | CH3 CH3 H H |
| R2 | CH3 H CH3 H |
| A. | α和β两种生育三烯酚互为同系物,β和γ两种生育三烯酚互为同分异构体 | |
| B. | 4种生育三烯酚均可使酸性高锰酸钾溶液褪色 | |
| C. | 4种生育三烯酚都难溶于水 | |
| D. | 1 mol δ生育三烯酚与溴水发生反应,理论上最多可消耗3 mol Br2 |
20.实验室需要480mL 0.1mol•L-1硫酸铜溶液,以下操作中正确的是( )
| A. | 称取7.86g硫酸铜,加入500mL水 | |
| B. | 称取12.0gCuSO4•5H2O,配制480mL溶液 | |
| C. | 称取8.0g硫酸铜,加入500mL水 | |
| D. | 称取12.5gCuSO4•5H2O,配制500mL溶液 |
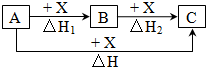 一定条件下A、B、C有如图所示的转化关系,且△H=△H1+△H2符合上述转化关系的A、C可能是①Fe、FeCl3 ②C、CO2 ③AlCl3、NaAlO2 ④NaOH、NaHCO3 ⑤S、SO3 ⑥Na2CO3、CO2( )
一定条件下A、B、C有如图所示的转化关系,且△H=△H1+△H2符合上述转化关系的A、C可能是①Fe、FeCl3 ②C、CO2 ③AlCl3、NaAlO2 ④NaOH、NaHCO3 ⑤S、SO3 ⑥Na2CO3、CO2( )