题目内容
下列物质性质与应用关系的描述正确的是( )
| A、稀硝酸具有强酸性,实验室可用其制取少量氢气 |
| B、铝具有强氧化性,生产上可用铝热反应制取一些金属 |
| C、氢氧化铝具有两性,医疗上可用其治疗胃酸过多 |
| D、钠具有强还原性,可用其与硫酸铜溶液反应来制取铜 |
考点:钠的化学性质,铝的化学性质,两性氧化物和两性氢氧化物
专题:
分析:A.硝酸具有强的氧化性,与金属反应得不到氢气;
B.铝为金属,不具有氧化性,具有强的还原性;
C.氢氧化铝能够与盐酸反应,消耗氢离子;
D.钠性质活泼,与盐溶液反应,先于水反应.
B.铝为金属,不具有氧化性,具有强的还原性;
C.氢氧化铝能够与盐酸反应,消耗氢离子;
D.钠性质活泼,与盐溶液反应,先于水反应.
解答:
解:A.硝酸具有强的氧化性,与金属反应得不到氢气,不能用硝酸制备氢气,故A错误;
B.用铝热反应制取一些金属,利用的是铝的还原性,故B错误;
C.氢氧化铝能够与盐酸反应,消耗氢离子,且碱性较弱,可以治疗胃酸过多,故C正确;
D.钠具有强还原性,与硫酸铜溶液反应生成氢氧化铜、硫酸钠和氢气,故D错误;
故选:C.
B.用铝热反应制取一些金属,利用的是铝的还原性,故B错误;
C.氢氧化铝能够与盐酸反应,消耗氢离子,且碱性较弱,可以治疗胃酸过多,故C正确;
D.钠具有强还原性,与硫酸铜溶液反应生成氢氧化铜、硫酸钠和氢气,故D错误;
故选:C.
点评:本题考查了元素化合物知识,熟悉相关物质的性质及用途是解题关键题目难度不大.

练习册系列答案
相关题目
下列物质与水反应生成强酸的是( )
| A、Na2O |
| B、NO2 |
| C、SO2 |
| D、SO3 |
下列说法中错误的是( )
| A、卤化氢中,HF沸点较高,是由于HF分子间存在氢键 |
| B、邻羟基苯甲醛的熔沸点比对羟基苯甲醛的熔沸点低 |
| C、氨水中有分子间氢键 |
| D、氢键X-H…Y的三个原子总在一条直线上 |
有关煤的叙述中不正确的是( )
| A、煤是工业上获得苯、甲苯、二甲苯等芳香烃的重要来源物质 |
| B、煤是多种有机物组成的混合物,内含煤焦油等成份 |
| C、煤除了含有碳元素外,还含有少量的N、H、O、S |
| D、工业上,煤的焦化可以获得洁净的燃料和多种化工原料 |
下列反应不属于消去反应的是( )
A、CH3CH2OH
| |||
B、CH3CHBrCH3+NaOH
| |||
C、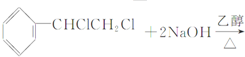  | |||
D、2CH3OH
|
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、使苯酚显紫色的溶液:NH4+、K+、SCN-、SO42- |
| B、使甲基橙变红色的溶液:Mg2+、K+、SO42-、NO3- |
| C、由水电离的c(OH-)=10-13mol?L-1的溶液中:Na+、Cl-、CO32-、NO3- |
| D、c(Fe2+)=1.0 mol?L-1溶液:H+、K+、Cl-、NO3- |
下列电池工作时,O2在正极放电的是( )
A、 锌锰电池 |
B、 氢燃料电池 |
C、 铅蓄电池 |
D、 镍镉电池 |
下列有关电化学装置完全正确的是( )
| A | B | C | D |
 |  |  |  |
| 铜的精炼 | 铁上镀银 | 防止Fe被腐蚀 | 构成铜锌原电池 |
| A、A | B、B | C、C | D、D |