题目内容
有七种物质:①甲烷 ②苯 ③聚乙烯 ④乙炔 ⑤1-丁烯 ⑥环己烷 ⑦甲苯,其中既能使酸性高锰酸钾溶液褪色,又能使溴水因发生反应而褪色的是( )
| A、①④⑤ | B、④⑤ |
| C、④⑤⑦ | D、③④⑤ |
考点:苯的性质,甲烷的化学性质,苯的同系物
专题:有机物的化学性质及推断
分析:既能使酸性高锰酸钾溶液褪色,又能使溴水因反应而褪色的有机物,应含有不饱和碳碳键或醛基,以此解答该题.
解答:
解:①甲烷为饱和烃,与酸性高锰酸钾或溴水都不反应,故①错误;
②苯结构特殊、性质稳定,与酸性高锰酸钾或溴水都不反应,故②错误;
③聚乙烯不含不饱和键,不能与酸性高锰酸钾或溴水反应,故③错误;
④2-丁炔含有碳碳三键,可与酸性高锰酸钾或溴水反应,故④正确;
⑤1-丁烯中含有碳碳双键,可与酸性高锰酸钾或溴水反应,故⑤正确;
⑥环己烷不含不饱和键,不能与酸性高锰酸钾或溴水反应,故⑥错误;
⑦甲苯可与酸性高锰酸钾反应,但与溴水不反应,故⑦错误.
故选B.
②苯结构特殊、性质稳定,与酸性高锰酸钾或溴水都不反应,故②错误;
③聚乙烯不含不饱和键,不能与酸性高锰酸钾或溴水反应,故③错误;
④2-丁炔含有碳碳三键,可与酸性高锰酸钾或溴水反应,故④正确;
⑤1-丁烯中含有碳碳双键,可与酸性高锰酸钾或溴水反应,故⑤正确;
⑥环己烷不含不饱和键,不能与酸性高锰酸钾或溴水反应,故⑥错误;
⑦甲苯可与酸性高锰酸钾反应,但与溴水不反应,故⑦错误.
故选B.
点评:本题考查有机物的结构和性质,侧重于有机物知识的综合考查,为高考常见题型,难度中等,注意把握常见有机物的官能团的性质.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
化学与社会、生活密切相关,下列说法错误的是( )
| A、市场上假酒销售时有发生,假酒的有毒成分主要是甲醇 |
| B、由石油分馏可获得汽油、煤油、柴油等,可用作燃料和煤油还可保存少量金属钠 |
| C、甲醛水溶液可以用来作食品防腐剂 |
| D、遵守《保护臭氧层维也纳公约》,限制生产和销售氟里昂可减少对大气臭氧层的破坏 |
下列有关物质的分类正确的是( )
| A、石油、煤、小苏打都是混合物 |
| B、烧碱、纯碱、碱石灰都是碱 |
| C、HNO3、NaOH、NaNO3都是电解质 |
| D、HCl、H2SO4、NaOH都是离子化合物 |
设NA表示阿伏伽德罗常数值,下列叙述正确的是( )
| A、常温下,1L pH=12的Ba(OH)2溶液中含有的OH-数为0.01NA |
| B、常温下,1L 0.1mol/L的CH3COOH溶液中含有的H+数为0.1NA |
| C、11.2 L乙烯、乙烷的混合气体中含有的碳原子数为NA |
| D、5.6 g Fe和足量盐酸完全反应,转移的电子数为0.3NA |
下列各项表达中不正确的是( )
| A、Be2+中的电子数和质子数之比一定为1:2 |
| B、D216O中,质量数之和是质子数之和的两倍 |
| C、在氮原子中,质子数为7而中子数不一定为7 |
D、Cl-的结构示意图为: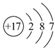 |

 A、B、C、D、E、F六种元素位于周期表前四周期且原子序数依次增大.①A元素的一种核素中子数是质子数的2倍;②基态B原子核外有两个未成对电子;③大气中C的游离态含量最高;④D原子基态核外电子运动状态共8种;⑤E、F原子序数相差3,基态E原子中有4个未成对屯子且全在同一能级内.
A、B、C、D、E、F六种元素位于周期表前四周期且原子序数依次增大.①A元素的一种核素中子数是质子数的2倍;②基态B原子核外有两个未成对电子;③大气中C的游离态含量最高;④D原子基态核外电子运动状态共8种;⑤E、F原子序数相差3,基态E原子中有4个未成对屯子且全在同一能级内.