题目内容
2.根据下列实验和现象,所得实验结论正确的是( )| 实验 | 现象 | 实验结论 | |
| A | 向某溶液中先滴加适量稀硝酸,再滴加少量BaCl2溶液 | 出现白色沉淀 | 原溶液中含有SO42-,SO32-,HSO3-中的一种或几种 |
| B | 将纯碱和硫酸反应生成的气体,通入一定浓度Na2SiO3溶液中 | 出现白色胶状沉淀 | 酸性:H2SO4>H2CO3>H2SiO3 |
| C | 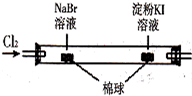 | 左边棉球变为橙色,右边棉球变为蓝色 | 氧化性:Cl2>Br2>I2 |
| D | 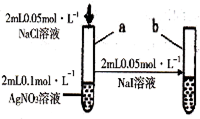 | 试管a出现白色沉淀,试管b出现黄色沉淀 | 溶度积:KSP(AgCl)>KSP(AgI) |
| A. | A | B. | B | C. | C | D. | D |
分析 A.硝酸具有强氧化性,先滴加硝酸酸化,可氧化SO32-、HSO3-;
B.根据强酸制备弱酸;
C.氯气可与NaBr、KI反应;
D.硝酸银过量,不发生沉淀转化.
解答 解:A.硝酸具有强氧化性,先滴加硝酸酸化,可氧化SO32-、HSO3-,且白色沉淀还可能为AgCl,原溶液可能存在银离子,而检验硫酸根离子应选盐酸酸化,故A错误;
B.根据强酸制备弱酸,可证明酸性:H2SO4>H2CO3>H2SiO3,故B正确;
C.氯气可与NaBr、KI反应,则该实验不能比较Br2、I2的氧化性,故C错误;
D.硝酸银过量,不发生沉淀转化,应向白色沉淀中加入碘化钠,故D错误.
故选B.
点评 本题考查化学实验方案的评价,为高频考点,涉及酸性比较、氧化性比较、离子检验及沉淀转化等,把握物质的性质及反应原理为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.下列电解质溶液有关叙述正确的是( )
| A. | 恒温条件下稀释氢氟酸时,HF的Ka增大,水的KW不变 | |
| B. | 向Mg(OH)2沉淀悬浊液中加入NH4Cl固体,c(Mg2+)、c(OH-)浓度均增大 | |
| C. | 0.1mol/LNaHCO3溶液中,c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| D. | 0.1mol/LNa2SO3溶液中,加入少量NaOH固体,c(SO32-)与c(Na+)均增大 |
6.下列物质的熔点,前者大于后者的是( )
| A. | 晶体硅、碳化硅 | B. | 氯化钠、甲苯 | C. | 氧化钠、氧化镁 | D. | 钾钠合金、钠 |
3. 我国“蛟龙”号载入潜水器进行第五次下潜试验,最大深度达到7062米,并完全返回.其动力电源是Al-AgO电池,原理如图所示.下列说法中正确的是( )
我国“蛟龙”号载入潜水器进行第五次下潜试验,最大深度达到7062米,并完全返回.其动力电源是Al-AgO电池,原理如图所示.下列说法中正确的是( )
 我国“蛟龙”号载入潜水器进行第五次下潜试验,最大深度达到7062米,并完全返回.其动力电源是Al-AgO电池,原理如图所示.下列说法中正确的是( )
我国“蛟龙”号载入潜水器进行第五次下潜试验,最大深度达到7062米,并完全返回.其动力电源是Al-AgO电池,原理如图所示.下列说法中正确的是( )| A. | Al电极是该电池的正极 | |
| B. | Ag在AgO/Ag电极上发生氧化反应 | |
| C. | 该电池负极反应是2Al-6e-+8OH-═2AlO2-+4H2O | |
| D. | AgO/Ag电极溶液中的pH减小 |
10.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A. | 62g白磷中含有2NA个白磷分子 | |
| B. | 1L 0.2mol/L Ba(NO3)2溶液中含有0.2NA个NO3- | |
| C. | 标准状况下,用MnO2和浓盐酸反应制取Cl2,当有4mol HCl被氧化时,生成2NA Cl2 | |
| D. | 25℃时,pH=7的NH4Cl和NH3•H2O的混合溶液中,0H-数10-7NA |
14.短周期元素X、Y、Z、W、Q在元素周期表中的位置如表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法中不正确的是( )
| X | Y | ||
| Z | W | Q |
| A. | 由Y与W形成的氧化物溶于水一定是强酸 | |
| B. | X与Y能形成两种常见的化合物 | |
| C. | Z与Q形成的物质能与H2在一定条件下反应 | |
| D. | X和Y均存在同素异形体 |
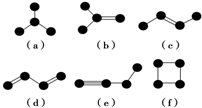 如图是由4个碳原子结合成的6种有机物(氢原子没有画出).
如图是由4个碳原子结合成的6种有机物(氢原子没有画出).
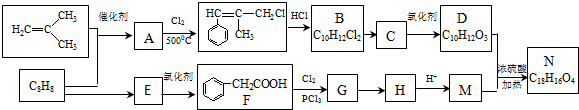
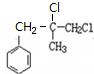 .
.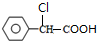 +2NaOH $→_{△}^{水}$
+2NaOH $→_{△}^{水}$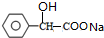 +NaCl+H2O.其反应类型为水解反应、中和反应.
+NaCl+H2O.其反应类型为水解反应、中和反应.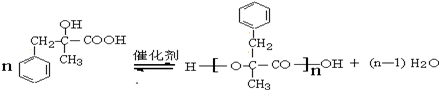 .
.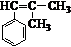 ,而不是
,而不是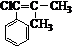 或
或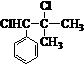 的原因是因为该条件下与双键相连的甲基上的氢原子更易取代.
的原因是因为该条件下与双键相连的甲基上的氢原子更易取代.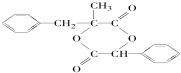 .
.