题目内容
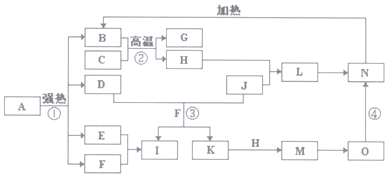
11.由短周期元素组成的单质A、B、C和甲、乙、丙、丁、戊五种化合物有如图所示转换关系.A是在地壳中含量最多的金属元素.请回答:
(1)物质的化学式为:乙NaAlO2丁AlCl3戊Al(OH)3;
(2)甲物质在工业上的一种重要用途:冶炼金属铝的原料或做耐火材料(坩埚等);
(3)A在元素周期表中的位置:第三周期ⅢA;
(4)A→乙+C反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
分析 A是地壳中含量最多的金属元素,则A为Al;Al与NaOH溶液反应生成单质C及乙,C为单质、乙为化合物,则C为H2、乙为NaAlO2;Al与单质B化合生成甲,甲能与氢氧化钠溶液、盐酸反应,则甲为两性氧化物Al2O3,B为O2;结合转化关系可知,丙为H2O、丁为AlCl3,丁与氨水反应生成戊为Al(OH)3,据此进行解答.
解答 解:A是地壳中含量最多的金属元素,则A为Al,Al与NaOH溶液反应生成单质C及乙,则C为H2,乙为NaAlO2.Al与单质B化合生成甲,甲能与氢氧化钠溶液、盐酸反应,则甲为Al2O3,B为O2,结合转化关系可知,丙为H2O,丁为AlCl3,丁与氨水反应生成戊为Al(OH)3,
(1)由上述分析可知,乙、丁、戊分别为NaAlO2、AlCl3、Al(OH)3,
故答案为:NaAlO2;AlCl3;Al(OH)3;
(2)甲为Al2O3,含金属元素Al,且熔点较高,则可冶炼金属铝的原料或做耐火材料(坩埚等),
故答案为:冶炼金属铝的原料或做耐火材料(坩埚等);
(3)A为Al元素,原子序数为13,位于周期表中第三周期ⅢA,
故答案为:第三周期ⅢA;
(4)A→乙+C的反应为Al与氢氧化钠溶液反应生成偏铝酸钠和水,该反应化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
点评 本题考查无机物的推断,题目难度中等,A的含量是推断突破口,把握Al及其化合物的性质为解答本题的关键,注意氧化铝的两性,试题有利于提高 学生的分析能力及逻辑推理能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.下列物质中氧元素的化合价正确的是( )
| A. | H2O中氧元素的化合价为-l | B. | Na2O2中氧元素的化合价为-2 | ||
| C. | NaOH中氧元素的化合价为-1 | D. | Na2O中氧元素的化合价为-2 |
2.(1)已知25℃时,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=2.5×10-9将浓度均为0.1mol•L-1的BaCl2溶液与Na2SO4溶液等体积混合,充分搅拌后过滤,滤液中C(Ba2+)=1×10-5mol•L-1.取100mL滤液与100mL 2mol•L-1的Na2SO4溶液混合,混合液中C(Ba2+)=1×10-10mol•L-1
(2)25℃醋酸的电离常数Ka=1.7×10-5mol•L-1 计算此温度下CH3COO-的水解平衡常数Kh=5.9×10-10mol•L-1.
| 阳离子 | Na+,Ba2+,NH4+ |
| 阴离子 | CH3COO-,Cl-,OH-,SO42- |
6.常温下,向浓HNO3中加入下列物质,反应最快、现象最明显的是( )
| A. | Al | B. | Cu | C. | Fe | D. | C |
3.对于反应:2SO2+O2?2SO3,当其他条件不变时,只改变一个条件,将生成SO3的反应速率的变化填入下表格里(填“增大”、“减小”或“不变”).
| 编号 | 改变的条件 | 生成的SO3的速率 |
| ① | 降低温度 | 减小 |
| ② | 升高温度 | 增大 |
| ③ | 增大O2的浓度 | 增大 |
| ④ | 恒容下充入Ne | 不变 |
| ⑤ | 压缩体积 | 增大 |
| ⑥ | 使用催化剂 | 增大 |
1.海水蕴藏着丰富的资源.下列有关海水综合利用的说法中,正确的是( )
| A. | 从海水中可提取食盐 | |
| B. | 海水蒸馏可得淡水 | |
| C. | 直接电解海水可得镁 | |
| D. | 从海水中得到淡水的方法有蒸馏法、电渗析法、离子交换法 |