题目内容
15.金刚石是典型的原子晶体,下列关于金刚石的说法中错误的是( )| A. | 晶体中不存在独立的“分子” | |
| B. | 碳原子间以共价键相结合 | |
| C. | 是硬度最大的物质之一 | |
| D. | 化学性质稳定,即使在高温下也不会与氧气发生反应 |
分析 A.金刚石是原子晶体,是由原子构成的;
B.非金属元素之间易形成共价键;
C.原子晶体硬度较大;
D.C单质在常温下较稳定,但高温下能与氧气反应生成碳的氧化物.
解答 解:A.金刚石是原子晶体,是由原子构成的,所以晶体中不存在独立的“分子”,故A正确;
B.金刚石中C原子之间以共用电子对形成共价键,故B正确;
C.原子晶体硬度较大,金刚石是原子晶体,其硬度较大,故C正确;
D.C原子最外层有4个电子,不易得电子也不易失电子,所以其单质在常温下较稳定,但高温下能与氧气反应生成碳的氧化物,故D错误;
故选D.
点评 本题考查金刚石组成、结构及其性质,为高频考点,以金刚石为例熟练掌握原子晶体构成微粒、晶胞结构,题目难度不大.

练习册系列答案
相关题目
3.根据对角线规则,下列物质的性质具有相似性的是( )
| A. | 硼和硅 | B. | 铝和铁 | C. | 铍和铝 | D. | 铜和金 |
6.阿司匹林(乙酰水杨酸,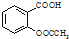 )是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:

主要试剂和产品的物理常数
请根据以上信息回答下列问题:
(1)制备阿司匹林时,要使用干燥的仪器的原因是防止乙酸酐水解.
(2)合成阿斯匹林时,最合适的加热方法是水浴加热.
(3)提纯粗产物中加入饱和NaHCO3溶液至没有CO2产生为止,再抽滤,则加饱和NaHCO3溶液的目的是使乙酰水杨酸与NaHCO3溶液作用转化为易溶于水的乙酰水杨酸钠,便于与聚合物分离.
另一种改进的提纯方法,称为重结晶提纯法.方法如下:

(4)改进的提纯方法中加热回流的装置如图所示
①使用温度计的目的是控制反应温度,防止温度过高,乙酰水杨酸受热分解.冷凝水的流进方向是b.(填“b”或“c”).
②重结晶提纯法所得产品的有机杂质要比原方案少的原因水杨酸易溶于乙酸乙酯,冷却结晶时大部分水杨酸仍溶解在乙酸乙酯中很少结晶出来.
(5)检验产品中是否含有水杨酸的化学方法是取少量结晶于试管中,加蒸馏水溶解,滴加FeCl3溶液,若呈紫蓝色,则含水杨酸.
(6)该学习小组在实验中原料用量:2.0g水杨酸、5.0mL醋酸酐(ρ=1.08g/cm3),最终称得产品m=2.2g,则所得乙酰水杨酸的产率为84.3%.
 )是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
主要试剂和产品的物理常数
| 名称 | 相对分子质量 | 熔点或沸点 (℃) | 水 |
| 水杨酸 | 138 | 158(熔点) | 微溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 反应 |
| 乙烯水杨酸 | 180 | 135(熔点) | 微溶 |
(1)制备阿司匹林时,要使用干燥的仪器的原因是防止乙酸酐水解.
(2)合成阿斯匹林时,最合适的加热方法是水浴加热.
(3)提纯粗产物中加入饱和NaHCO3溶液至没有CO2产生为止,再抽滤,则加饱和NaHCO3溶液的目的是使乙酰水杨酸与NaHCO3溶液作用转化为易溶于水的乙酰水杨酸钠,便于与聚合物分离.
另一种改进的提纯方法,称为重结晶提纯法.方法如下:

(4)改进的提纯方法中加热回流的装置如图所示

①使用温度计的目的是控制反应温度,防止温度过高,乙酰水杨酸受热分解.冷凝水的流进方向是b.(填“b”或“c”).
②重结晶提纯法所得产品的有机杂质要比原方案少的原因水杨酸易溶于乙酸乙酯,冷却结晶时大部分水杨酸仍溶解在乙酸乙酯中很少结晶出来.
(5)检验产品中是否含有水杨酸的化学方法是取少量结晶于试管中,加蒸馏水溶解,滴加FeCl3溶液,若呈紫蓝色,则含水杨酸.
(6)该学习小组在实验中原料用量:2.0g水杨酸、5.0mL醋酸酐(ρ=1.08g/cm3),最终称得产品m=2.2g,则所得乙酰水杨酸的产率为84.3%.
3.下列微粒中立体构型是平面三角形的是( )
| A. | NH3 | B. | BCl3 | C. | PCl3 | D. | H2O |
10.下列叙述错误的是( )
| A. | 金属钠在自然界中能以游离态存在 | B. | 钠燃烧时发出黄色的火焰 | ||
| C. | 钠能与S、Cl2等非金属反应 | D. | 钠在空气中燃烧生成过氧化钠 |
20.将4.6g金属钠投入到足量水中,得到ag溶液;将4.8g金属镁投入到足量盐酸中,得bg溶液.若水的质量与盐酸的质量相等,则反应后两溶液的质量关系式是( )
| A. | a=b | B. | a<b | C. | a>b | D. | 无法判断 |
4.对电解质概念的理解正确的是( )
| A. | 在水溶液中或熔融状态下能导电的物质 | |
| B. | 凡在水中能生成离子因而能导电的物质 | |
| C. | 氧化钠溶于后水溶液能导电,但溶液中的离子并非本身电离,因而氧化钠是非电解质 | |
| D. | 在水溶液里或熔融状态下本身能电离出阳离子和阴离子,因而是能导电的化合物 |