题目内容
12.一氧化碳和氢气的体积比VCO:VH2=51:14时(标准状况)混合,才能配成密度为1g/升的混合气体.分析 根据M=ρM计算出混合气体的评价摩尔质量,然后设出一氧化碳和氢气的物质的量,结合评价摩尔质量列式计算即可.
解答 解:标况下1g/L的混合气体的评价摩尔质量为:1g/L×22.4L/mol=22.4g/mol,
设混合气体中CO、H2的物质的量分别为x、y,
则:$\frac{28g/mol×x+2g/mol×y}{x+y}$=22.4g/mol,
整理可得x:y=51:14,
相同条件下气体体积之比等于物质的量之比,所以一氧化碳和氢气的体积比V(CO):V(H2)=51:14,
故答案为:51:14.
点评 本题考查了物质的量计算,题目难度不大,明确物质的量与气体摩尔体积、摩尔质量之间的关系即可答,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
2.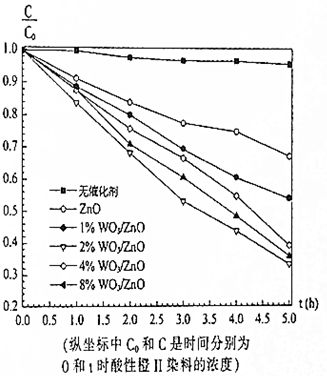 在紫外光照射下,利用WO3/ZnO光催化剂降解酸性橙Ⅱ染料废水的实验所得曲线如图.下列说法错误的是( )
在紫外光照射下,利用WO3/ZnO光催化剂降解酸性橙Ⅱ染料废水的实验所得曲线如图.下列说法错误的是( )
 在紫外光照射下,利用WO3/ZnO光催化剂降解酸性橙Ⅱ染料废水的实验所得曲线如图.下列说法错误的是( )
在紫外光照射下,利用WO3/ZnO光催化剂降解酸性橙Ⅱ染料废水的实验所得曲线如图.下列说法错误的是( )| A. | 不加催化剂时,紫外光照射降解酸性橙Ⅱ染料废水反应速率较慢 | |
| B. | 单一ZnO材料也是降解酸性橙Ⅱ染料废水的催化剂 | |
| C. | 2%WO3/ZnO的催化效果最好 | |
| D. | 由图中可以看出,光降解酸性橙Ⅱ染料是一个可逆反应 |
20.短周期主族元素A、B、X、Y的原子序数依次增大,A、B、X、Y原子的最外层电子数之和为18,A原子的最外层电子数是其内层电子数的2倍,X2+与B2-具有相同的电子层结构.下列说法正确的是( )
| A. | 单质的沸点:B>X | |
| B. | B、X、Y的原子半径大小顺序为:X>Y>B | |
| C. | A的最高价氧化物对应的水化物的酸性强于Y的 | |
| D. | B分别与X、Y形成的化合物中化学键类型相同 |
7.醇是一类非常重要的有机化合物,下列关于醇的说话中,不正确的是( )
| A. | 醇的官能团委羟基(-OH),它与氢氧根(OH-)具有相同的结构 | |
| B. | 工业酒精中往往含有甲醇,因此不可用来勾兑白酒 | |
| C. | 乙醇能够以任意比溶解于水,所以酒厂可以勾兑各种浓度的酒 | |
| D. | 乙醇,乙二醇,丙三醇分别属于一元醇、二元醇、三元醇 |
17.设NA为阿伏伽德罗常数的数值,下列有关叙述正确的是( )
| A. | 100g质量分数为46%的乙醇溶液中所含的氢原子数为12NA | |
| B. | pH=1的硫酸溶液中含有的SO42-数目为0.05NA | |
| C. | 向1L0.3mol•L-1NaOH溶液中通入0.2molCO2,溶液中CO32-和HCO3-的数目均为0.1NA | |
| D. | 0.2molNH3与0.3molO2在催化剂的作用下加热充分反应,所得NO的分子数为0.2NA |
6.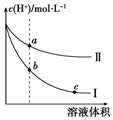 某温度下,等体积、c(H+)相同的盐酸和醋酸溶液分别加水稀释,溶液中的c(H+)随溶液体积变化的曲线如图所示.据图判断下列说法正确的是( )
某温度下,等体积、c(H+)相同的盐酸和醋酸溶液分别加水稀释,溶液中的c(H+)随溶液体积变化的曲线如图所示.据图判断下列说法正确的是( )
 某温度下,等体积、c(H+)相同的盐酸和醋酸溶液分别加水稀释,溶液中的c(H+)随溶液体积变化的曲线如图所示.据图判断下列说法正确的是( )
某温度下,等体积、c(H+)相同的盐酸和醋酸溶液分别加水稀释,溶液中的c(H+)随溶液体积变化的曲线如图所示.据图判断下列说法正确的是( )| A. | 曲线Ⅱ表示的是盐酸的变化曲线 | |
| B. | b点溶液的导电性比c点溶液的导电性强 | |
| C. | 取等体积的a点、b点对应的溶液,消耗的NaOH的量相同 | |
| D. | b点酸的总浓度大于a点酸的总浓度 |
3.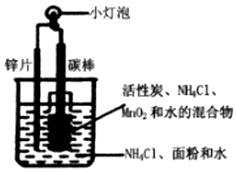 干电池模拟实验装置如图.下列说法不正确的是( )
干电池模拟实验装置如图.下列说法不正确的是( )
 干电池模拟实验装置如图.下列说法不正确的是( )
干电池模拟实验装置如图.下列说法不正确的是( )| A. | 碳棒作正极,锌片作负极 | |
| B. | 电流方向从碳棒流向锌片,电子则相反 | |
| C. | NH4Cl是电解质,在锌片逐渐消耗过程中 MnO2不断被还原 | |
| D. | 该电池是二次电池,该废旧电池中锌可回收 |
4.下列制定反应的离子方程式正确的是( )
| A. | Cu与浓硝酸反应制备NO2:3Cu+8H++2NO3-═3Cu2++2NO2↑+4H2O | |
| B. | Na2S2O3溶液吸收水中多余的Cl2:4Cl2+S2O32-+5H2O=10H++2SO42-+8Cl- | |
| C. | 用惰性电极电解CuSO4溶液:2Cu2++4OH-$\frac{\underline{\;通电\;}}{\;}$2Cu↓+O2↑+2H2O | |
| D. | 向明矾溶液中滴入氢氧化钡溶液至沉淀的物质的量最大:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |