题目内容
下列实验方案不可行的是( )
| A、用稀盐酸清洗做焰色反应的铂丝 |
| B、金属钠保存在煤油中 |
| C、用湿润的淀粉KI试纸靠近试剂瓶口检验Cl2是否收集满 |
| D、除去粗盐溶液中的Ca2+、SO42-:先加Na2CO3溶液后加BaCl2溶液 |
考点:化学实验方案的评价
专题:
分析:A.根据盐酸的性质分析,盐酸可以溶解氧化物等杂质且易挥发;
B.钠能与空气中的水和氧气反应,又钠的密度比水略小;
C.氯气与KI反应生成碘单质;
D.加碳酸钠要放在加氯化钡之后,可以将过量的钡离子沉淀.
B.钠能与空气中的水和氧气反应,又钠的密度比水略小;
C.氯气与KI反应生成碘单质;
D.加碳酸钠要放在加氯化钡之后,可以将过量的钡离子沉淀.
解答:
解:A.用盐酸洗涤铂丝,再灼烧至跟酒精灯火焰颜色相同后使用,去除了其它离子的干扰,且HCL受热以后会挥发,无残留,故A正确;
B.钠能与空气中的水和氧气反应,又钠的密度比水略小,故钠保存在煤油中,或用石蜡密封保存,故B正确;
C.氯气与KI反应生成碘单质,淀粉遇碘变蓝,则用湿润的淀粉KI试纸检验Cl2是否收集满,故C正确;
D.钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,故D错误.
故选D.
B.钠能与空气中的水和氧气反应,又钠的密度比水略小,故钠保存在煤油中,或用石蜡密封保存,故B正确;
C.氯气与KI反应生成碘单质,淀粉遇碘变蓝,则用湿润的淀粉KI试纸检验Cl2是否收集满,故C正确;
D.钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,故D错误.
故选D.
点评:本题考查化学实验方案的评价,涉及焰色反应、物质的保存、物质的检验等知识点,难度不大,注意焰色反应洗涤铂丝用稀盐酸,不用稀硫酸.

练习册系列答案
相关题目
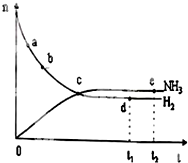 合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g)△H<0,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )
合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g)△H<0,673K,30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )| A、点a的逆反应速率比点b的大 |
| B、点c处反应达到平衡 |
| C、点d(t1时刻)和点e(t2时刻)处H2的转化率相同 |
| D、点d(t1时刻)和点e(t2时刻)处n(N2)不一样 |
下列每组中各有三对物质,他们都能用分液漏斗分离的是( )
| A、乙酸乙酯和水,酒精和水,植物油和水 |
| B、四氯化碳和水,溴苯和水,硝基苯和水 |
| C、甘油和水,乙酸和水,乙酸和乙醇 |
| D、酒精和水,苯和水,己烷和水 |


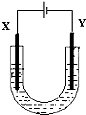 如图是用石墨和铁作电极电解饱和食盐水的装置,请填空:
如图是用石墨和铁作电极电解饱和食盐水的装置,请填空: