题目内容
下列反应的现象描述与离子方程式都正确的是( )
| A、金属镁与稀醋酸反应:有气泡逸出 Mg+2H+═Mg2++H2↑ | ||||
B、氢氧化钡溶液与稀硫酸反应:有白色沉淀生成 Ba2++SO
| ||||
| C、少量金属钠加到冷水中:有气泡逸出:2Na+2H2O═2Na++2OH-+H2↑ | ||||
D、NaHCO3溶液中加入过量的Ba(OH)2溶液:有白色沉淀产生 2HCO
|
考点:离子方程式的书写
专题:离子反应专题
分析:A、醋酸为弱酸,应写成化学式;
B、漏掉一组离子反应,相关离子要符合组成之比;
C、钠与水电离出的氢离子之间发生置换反应;
D、设NaHCO3为1mol,完全反应需要1molBa(OH)2,以此分析离子方程式的正误.
B、漏掉一组离子反应,相关离子要符合组成之比;
C、钠与水电离出的氢离子之间发生置换反应;
D、设NaHCO3为1mol,完全反应需要1molBa(OH)2,以此分析离子方程式的正误.
解答:
解:A、醋酸为弱酸,应写成化学式,正确的离子方程式为 Mg+2CH3COOH=2CH3COO-+Mg2++H2↑,故A错误;
B、漏掉一组离子反应,相关离子要符合组成之比,正确的离子方程式为2H++SO42-+Ba2++2OH-═2H2O+BaSO4↓,故B错误;
C、钠与水电离出的氢离子之间的置换反应,离子方程式为2Na+2H2O═2Na++2OH-+H2↑,故C正确;
D、设NaHCO3为1mol,完全反应需要1molBa(OH)2,反应生成1molBaCO3,溶液中无CO32-离子剩余,正确的离子方程式为HCO3-+Ba2++OH-═BaCO3↓+H2O,故D错误;
故选C.
B、漏掉一组离子反应,相关离子要符合组成之比,正确的离子方程式为2H++SO42-+Ba2++2OH-═2H2O+BaSO4↓,故B错误;
C、钠与水电离出的氢离子之间的置换反应,离子方程式为2Na+2H2O═2Na++2OH-+H2↑,故C正确;
D、设NaHCO3为1mol,完全反应需要1molBa(OH)2,反应生成1molBaCO3,溶液中无CO32-离子剩余,正确的离子方程式为HCO3-+Ba2++OH-═BaCO3↓+H2O,故D错误;
故选C.
点评:本题考查离子方程式的书写,题目难度不大,注意从化学式、离子符号、电荷守恒以及是否符合反应实际的角度分析.

练习册系列答案
相关题目
若某电能与化学能的转化装置中发生的反应总离子方程式为Cu+2H+=Cu2++H2↑,则关于该装置的下列说法正确的是( )
| A、该装置可能是原电池,也可能是电解池 |
| B、该装置只能是电解池,且金属铜为该电解池的阳极 |
| C、该装置只能是电解池,电解质溶液不可能是盐酸 |
| D、该装置只能是原电池,且电解质溶液为硝酸 |
下列各选项的分类中,后者包括前者的是( )
| A、化合物,电解质 |
| B、分子,原子 |
| C、碱,化合物 |
| D、纯净物,盐 |
下列离子方程式不正确的是( )
| A、氢氧化铁溶于氢碘酸中:2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O |
| B、明矾溶液中加入氢氧化钡溶液,使其产生沉淀的物质的量达最大值:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O |
| C、Mg(HCO3)2溶液中加入过量石灰水:Mg2++2HCO3-+2Ca2++4OH-=2CaCO3↓+2H2O+Mg(OH)2↓ |
| D、向100mL 0.1mol/L的FeBr2溶液中通入0.012mol Cl2:10Fe2++14Br-+12Cl2=10Fe3++7Br2+24Cl- |
设NA代表阿伏伽德罗常数,下列说法正确的是( )
| A、22.4LNe含有NA个Ne分子 |
| B、1.7 g氨气所含有的电子数目为10NA |
| C、在H2O2+Cl2=2HCl+O2反应中,每生成32g氧气,则转移NA个电子 |
| D、常温常压下,16g O3含有的氧原子数为NA |
下列说法正确的是( )
| A、同一元素各核素的质量数不同,但它们的化学性质几乎完全相同 | ||||||
| B、任何元素的原子都是由核外电子和核内中子、质子构成的 | ||||||
| C、钠原子失去一个电子后,它的电子数与氖原子相同,变成10e-微粒 | ||||||
D、
| ||||||
E、
|
在标况下,若VL甲烷中含有的原子总数为a,则阿伏加德罗常数可表示为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
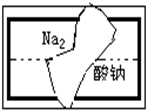 某研究性学习小组在整理实验室的化学试剂时,发现一盛有无色溶液的试剂瓶标签破损(如图),请你根据已掌握的知识,对该试剂可能是什么物质的溶液作出三种猜想,并设计实验验证,写出每一种猜想的实验操作、现象和结论.
某研究性学习小组在整理实验室的化学试剂时,发现一盛有无色溶液的试剂瓶标签破损(如图),请你根据已掌握的知识,对该试剂可能是什么物质的溶液作出三种猜想,并设计实验验证,写出每一种猜想的实验操作、现象和结论.