题目内容
18.实验室鉴别庚烷、1-庚烯和甲苯,所采用的试剂可以是下列中的( )| A. | 溴水石蕊溶液 | B. | 氢氧化钠溶液和溴水 | ||
| C. | 溴水和高锰酸钾酸性溶液 | D. | 高锰酸钾溶液 |
分析 烷烃性质稳定不能与溴水、酸性的高锰酸钾反应,烯烃能够使溴水、酸性的高锰酸钾反应,甲苯与溴水不反应,能够被酸性的高锰酸钾氧化,据此解答.
解答 解:庚烷性质稳定不能与溴水、酸性高锰酸钾反应,加入溴水、酸性高锰酸钾,溶液都不褪色;
庚烯能够与溴水发生加成反应使溴水褪色,能够被酸性的高锰酸钾氧化,使高锰酸钾褪色;
甲苯与溴水不反应,能够被酸性的高锰酸钾氧化,使高锰酸钾褪色;
所以为鉴别三种物质,取三种物质各少许放入试管,分别加入溴水,能够使溴水褪色的1-庚烯,没有现象的庚烷和甲苯;
然后取剩余两种液体,分别加入酸性的高锰酸钾,溶液褪色的为甲苯,无现象的为庚烷;
故选:C.
点评 本题考查了物质的鉴别,熟悉烷烃、烃、甲苯的结构及性质是解题关键,题目难度不大.

练习册系列答案
相关题目
8.光导纤维的主要成分是二氧化硅,下列关于二氧化硅的说法正确的是( )
| A. | 二氧化硅能与水反应 | |
| B. | 用二氧化硅制取单质硅,当生成2.24 L(标准状况下)气体时,得到2.8g硅 | |
| C. | 二氧化硅属于传统的无机非金属材料 | |
| D. | 二氧化硅不能与碳酸钠溶液发生反应,但在高温下能与碳酸钠固体发生反应 |
9.${\;}_{20}^{40}$Ca和 ${\;}_{19}^{40}$K的中子数( )
| A. | 大于 | B. | 小于 | C. | 等于 | D. | 不能肯定 |
6.关于原子序数为53的元素,以下说法正确的是( )
| A. | 位于第六周期 | B. | 是金属元素 | ||
| C. | 最外电子层含有6个电子 | D. | 属于卤族元素 |
3.某离子反应中共有H2O、ClO-、NH4+、H+、N2、Cl-六种微粒.其中C(ClO-)随反应进行逐渐减小.下列判断错误的是( )
| A. | 该反应的还原剂是NH4+ | |
| B. | 消耗1mol氧化剂,转移2mol电子 | |
| C. | 氧化剂与还原剂的物质的量之比是2:3 | |
| D. | 反应后溶液酸性明显增强 |
7.使用石油热裂解的副产物CH4来制取CO和H2,其生产流程如图:
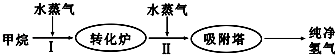
(1)工业上常利用反应Ⅰ产生的CO和H2合成可再生能源甲醇.
①已知CO(g)、CH3OH(l)的燃烧热分别为283.0kJ•mol-1和726.5kJ•mol-1,则CH3OH(l)不完全燃烧生成CO(g)和H2O(l)的热化学方程式为CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-443.5kJ•mol-1.
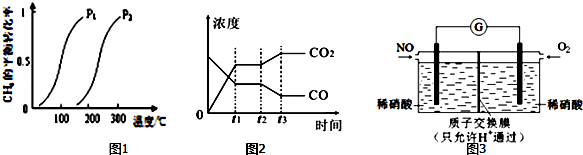
此流程的第Ⅰ步反应为:CH4(g)+H2O(g)?CO(g)+3H2(g),一定条件下CH4的平衡转化率与温度、压强的关系如图1.则P1<P2.(填“<”、“>”或“=”)100℃时,将1mol CH4和2mol H2O通入容积为10L的恒容密闭容器中,达到平衡时CH4的转化率为0.5.此时该反应的平衡常数K=2.25×10-2.
(3)此流程的第Ⅱ步反应CO(g)+H2O(g)?CO2(g)+H2(g),的平衡常数随温度的变化如表:
从上表可以推断:该反应是放热反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol/L,在该条件下,反应达到平衡时,CO的转化率为75%.图2表示该反应在t1时刻达到平衡、在t2时刻因改变某个条件引起浓度变化的情况:图2中t2时刻发生改变的条件是降低温度.增加水蒸汽的量或减少氢气的量(写出一种).
(4)某化学兴趣小组构想将NO转化为HNO3(NO3-),装置如图3,电极为多孔惰性材料.则负极的电极反应式是2H2O+NO-3e-=NO3-+4H+.

(1)工业上常利用反应Ⅰ产生的CO和H2合成可再生能源甲醇.
①已知CO(g)、CH3OH(l)的燃烧热分别为283.0kJ•mol-1和726.5kJ•mol-1,则CH3OH(l)不完全燃烧生成CO(g)和H2O(l)的热化学方程式为CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-443.5kJ•mol-1.
此流程的第Ⅰ步反应为:CH4(g)+H2O(g)?CO(g)+3H2(g),一定条件下CH4的平衡转化率与温度、压强的关系如图1.则P1<P2.(填“<”、“>”或“=”)100℃时,将1mol CH4和2mol H2O通入容积为10L的恒容密闭容器中,达到平衡时CH4的转化率为0.5.此时该反应的平衡常数K=2.25×10-2.
(3)此流程的第Ⅱ步反应CO(g)+H2O(g)?CO2(g)+H2(g),的平衡常数随温度的变化如表:
| 温度/℃ | 400 | 500 | 830 |
| 平衡常数K | 10 | 9 | 1 |
(4)某化学兴趣小组构想将NO转化为HNO3(NO3-),装置如图3,电极为多孔惰性材料.则负极的电极反应式是2H2O+NO-3e-=NO3-+4H+.

8.某气体由烯烃和炔烃混合而成,经测定其密度为同条件下H2的13.5倍,则下列说法中正确的是( )
| A. | 混合气体中一定没有乙炔 | B. | 混合气体中一定有乙稀 | ||
| C. | 混合气体可能由乙炔和丙烯组成 | D. | 混合气体一定由乙烯和乙炔组成 |