题目内容
16.(1)用“双线桥”表示电子转移的方向和数目:2Na2O2+2H2O═4NaOH+O2↑每消耗3molNa2O2转移电子为3mol,O2是氧化产物.写出Na2O2的一个用途:供氧剂.
(2)SiO2是玻璃的成分之一,用化学方程式说明为什么盛碱的试剂瓶不用玻璃塞?SiO2+2NaOH=Na2SiO3+H2O.
分析 (1)2Na2O2+2H2O═4NaOH+O2↑中只有O元素的化合价变化,过氧化钠为氧化剂也为还原剂;
(2)二氧化硅与碱反应生成具有粘合性的硅酸钠,则不能使用玻璃塞.
解答 解:(1)2Na2O2+2H2O═4NaOH+O2↑中只有O元素的化合价变化,过氧化钠为氧化剂也为还原剂,该反应转移2e-,“双线桥”表示电子转移的方向和数目为 ,每消耗3molNa2O2转移电子为3mol,失去电子被氧化,则O2是氧化产物,Na2O2的一个常见用途为作供氧剂,
,每消耗3molNa2O2转移电子为3mol,失去电子被氧化,则O2是氧化产物,Na2O2的一个常见用途为作供氧剂,
故答案为: ;3;O2;供氧剂;
;3;O2;供氧剂;
(2)二氧化硅与碱反应生成具有粘合性的硅酸钠,则不能使用玻璃塞,发生的反应为SiO2+2NaOH=Na2SiO3+H2O,故答案为:SiO2+2NaOH=Na2SiO3+H2O.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应的应用,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.下列物质一定属于同系物的是( )


| A. | ④和⑥ | B. | ①、②和③ | C. | ④、⑥和⑧ | D. | ⑤和⑦ |
4.分类是学习和研究化学的重要方法,下列分类合理的是( )
| A. | H2SO4和NaHSO4都属于酸 | B. | 火碱和纯碱都属于碱 | ||
| C. | KOH和NH3•H2O都属于电解质 | D. | Na2O和Na2O2都属于碱性氧化物 |
1.Cl2在70℃的NaOH水溶液中,能同时发生两个自身氧化还原反应,反应完全后测得溶液中NaClO和NaClO3的物质的量比为6:1,则溶液中NaCl和NaClO的物质的量之比为( )
| A. | 9:4 | B. | 6:1 | C. | 7:6 | D. | 11:6 |
8.下列离子或分子能够在指定的分散系中大量共存的是( )
| A. | 与铝反应生成大量氢气的溶液中:Mg2+、K+、HCO3-、NO3- | |
| B. | 0.1mol/L的NaNO3溶液中:K+、I-、Cl-、SO42- | |
| C. | 铁与稀硫酸反应后的溶液中:[Fe(CN)6]3-、NH4+、Cl-、NO3- | |
| D. | 空气中:SO2、NO、N2、NH3 |
6.下列实验能达到实验目的且符合安全要求的是( )
| A. | 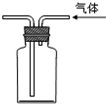 利用排空法收集CO2 | B. | 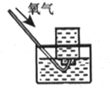 收集氧气 | ||
| C. | 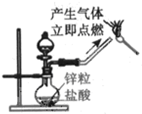 制备并检验氢气的可燃性 | D. | 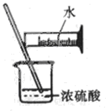 浓硫酸稀释 |
 化合物AX3和单质X2在一定条件下反应可生成化合物AX5.回答下列问题:
化合物AX3和单质X2在一定条件下反应可生成化合物AX5.回答下列问题: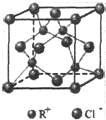 RCl常用作有机合成催化剂,并用于颜料,防腐等工业.R+中所有电子正好充满K、L、M三个电子层,它与Cl-形成的晶体结构如图所示.R的元素符号是Cu,每个Cl-周围最近的Cl-有12个.
RCl常用作有机合成催化剂,并用于颜料,防腐等工业.R+中所有电子正好充满K、L、M三个电子层,它与Cl-形成的晶体结构如图所示.R的元素符号是Cu,每个Cl-周围最近的Cl-有12个.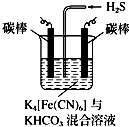 铁及其化合物在工农业生产、环境保护等领域中有着重要的作用.
铁及其化合物在工农业生产、环境保护等领域中有着重要的作用.