题目内容
8.运用元素周期律分析下列推断,其中错误的是( )| A. | 铍的最高价氧化物的水化物可能具有两性 | |
| B. | 砹单质是有色固体,砹化氢很不稳定,砹化银是有色难溶于水且感光性很强的固体 | |
| C. | 硫酸锶难溶于水,但易溶于盐酸 | |
| D. | 砷的最高价氧化物的水化物是一种强酸 |
分析 A.Be与Al位于对角线位置,性质相似;
B.卤素单质的状态、颜色从上到下由气到固,颜色加深,非金属性从上到下减小,砹化银难溶于水;
C.由硫酸钙不与盐酸反应可知硫酸锶的性质;
D.砷的最高价氧化物的水化物比磷酸的弱.
解答 解:A.Be与Al位于对角线位置,性质相似,氢氧化铝具有两性,则铍的最高价氧化物的水化物可能具有两性,故A正确;
B.卤素单质的状态、颜色从上到下由气到固,颜色加深,非金属性从上到下减小,砹化银难溶于水,可知砹单质是有色固体,砹化氢很不稳定,砹化银是有色难溶于水且感光性很强的固体,故B正确;
C.由硫酸钙不与盐酸反应可知,硫酸锶难溶于水,难溶于盐酸,故C错误;
D.砷的最高价氧化物的水化物比磷酸的弱,磷酸为中强酸,则砷酸为弱酸,故D错误;
故选CD.
点评 本题考查位置、结构及性质的应用,为高频考点,把握元素周期律为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
18.AgCl和BaSO4的溶解度随温度的变化曲线如图所示.下列说法不正确的是( )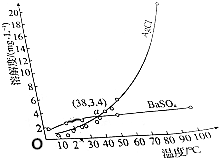

| A. | a点时,AgCl和BaSO4饱和溶液的密度基本相同 | |
| B. | AgCl的溶解是吸热过程 | |
| C. | 室温时,向等体积的饱和AgCl和BaSO4溶液中分别加入足量的浓BaCl2溶液,析出BaSO4沉淀的质量比AgCl多 | |
| D. | 可以用重结晶的方法分离AgCl和BaSO4 |
19.在25℃时,在水中通入氯化氢气体,当溶液的pH等于3时,此时由水本身电离出的c(H+)是(mol•L-1)( )
| A. | 10-3 | B. | 10-7 | C. | 10-11 | D. | 10-14 |
16.下列说法正确的是( )
| A. | 将FeCl3溶液加热蒸干,可得到FeCl3固体 | |
| B. | 将PH=9的KOH溶液稀释1000倍后,其PH=6 | |
| C. | 用NaOH溶液滴定醋酸溶液时,不宜选用甲基橙作指示剂 | |
| D. | 碳酸溶液中氢离子浓度是碳酸根离子浓度的二倍 |
3.下列有关实验说法中,正确的是( )
| A. | 用浓硝酸做试剂比较铁和铜的金属活动性 | |
| B. | 使用干燥洁净玻璃棒将氯水滴在干燥pH试纸上,测定氯水的pH | |
| C. | 欲检验Br-的存在,可在溶液中先加入氯水、再加入CCl4,振荡、静置,观察下层溶液显橙红色 | |
| D. | 氢氧化铁胶体在直流电场中,一段时间阴极附近红褐色加深,说明胶体带正电荷 |
仅依据下表给出的物理量X和Y,其中不能求出物质的量的是
A | B | C | D | |
X | 物质中的粒子数 | 标准状况下的 气体摩尔体积 | 固体的体积 | 溶液中溶质的 物质的量浓度 |
Y | 阿伏加德罗常数 | 标准状况下 气体的体积 | 固体的密度 | 溶液体积 |
14.下列关于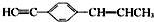 的说法正确的是( )
的说法正确的是( )
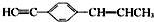 的说法正确的是( )
的说法正确的是( )| A. | 所有碳原子有可能都在同一个平面上 | |
| B. | 最多可能有9个碳原子在同一平面上 | |
| C. | 只能有4个碳原子在同一直线上 | |
| D. | 有7个碳原子可能在同一条直线上 |
15.下列各组物质中,属于同系物的是( )
| A. | HCOOCH3、CH3COOH | B. | 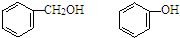 | ||
| C. | C15H31COOH、C17H35COOH | D. | 乙醇、丙三醇 |
 的
的