题目内容
16.下列说法正确的是( )| A. | 将FeCl3溶液加热蒸干,可得到FeCl3固体 | |
| B. | 将PH=9的KOH溶液稀释1000倍后,其PH=6 | |
| C. | 用NaOH溶液滴定醋酸溶液时,不宜选用甲基橙作指示剂 | |
| D. | 碳酸溶液中氢离子浓度是碳酸根离子浓度的二倍 |
分析 A、根据三氯化铁在溶液中存在水解平衡,从平衡移动的角度分析并解答该题;
B、将PH=9的KOH溶液无限稀释,溶液仍然是碱性的;
C、氢氧化钠和醋酸反应恰好反应生成的盐是强碱弱酸盐,盐水解显碱性,应选择碱性条件下变色的指示剂;
D、碳酸是弱酸,不能完全电离,二级电离远远小于一级电离.
解答 解:A、在FeCl3溶液中,Fe3+发生水解生成Fe(OH)3:FeCl3+3H2O?Fe(OH)3+3HCl,由于加热蒸发,使HCl挥发,破坏平衡,使平衡不断向右移动,结果生成Fe(OH)3,又由于灼热发生2Fe(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2O,使Fe(OH)3分解生成Fe2O3,故A错误;
B、将PH=9的KOH溶液稀释1000倍后,其pH接近于7,但是仍然大于7,故B错误;
C、氢氧化钠和醋酸反应恰好反应生成的盐是强碱弱酸盐,盐水解显碱性,应选择碱性条件下变色的指示剂,不能选择甲基橙,应选择酚酞指示剂,故C正确;
D、碳酸是弱酸,不能完全电离,二级电离远远小于一级电离,氢离子浓度远大于碳酸根离子浓度的2倍,故D错误.
故选C.
点评 本题考查盐的水解原理应用、弱电解质电离、溶液的稀释以及酸碱中和滴定等知识,B选项注意碱无限稀释接近中性的特点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.室温下,向10mL 0.1mol/L NaOH溶液中加入0.1mol•L-1的一元酸 HA溶液pH的变化曲线如图所示(横坐标单位是mL).下列说法不正确的是( )
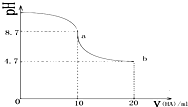

| A. | a点所示溶液中有c(Na+)>c(A-)>c(HA)>c(H+) | |
| B. | a、b两点曲线之间某时刻的溶液中有c(Na+)=c(A-) | |
| C. | a、b两点所示溶液中水的电离程度相同 | |
| D. | b点所示溶液中有 2c(Na+)=c(A-)+c(HA) |
7.下列事实不能用勒夏特列原理解释的是( )
| A. | 红棕色NO 2加压后颜色先变深后变浅 2NO2?N2O4 | |
| B. | 实验室中常用排饱和食盐水的方法收集氯气 | |
| C. | SO2催化氧化成SO3的反应,使用过量的空气以提高二氧化硫的利用率 | |
| D. | H2、I2、HI平衡混合气体加压后颜色变深 |
1.“嫦娥一号”的四大科学目标之一是探测下列14种元素在月球上的含量和分布:He、Th(钍)、U(铀)、O、Si、Mg、Al、Ca、Fe、Ti(钛)、Na、Mn、Cr(铬)、Gd(钆),其中属于主族元素的有( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
8.运用元素周期律分析下列推断,其中错误的是( )
| A. | 铍的最高价氧化物的水化物可能具有两性 | |
| B. | 砹单质是有色固体,砹化氢很不稳定,砹化银是有色难溶于水且感光性很强的固体 | |
| C. | 硫酸锶难溶于水,但易溶于盐酸 | |
| D. | 砷的最高价氧化物的水化物是一种强酸 |
3.已知:2SO2(g)+O2(g)?2SO3(g)+Q(Q>0),往密闭容器中加入2molSO2、1milO2,下列说法正确的是( )
| A. | 充分反应后放出热量为Q | |
| B. | 增大压强,平衡右移,Q值变大 | |
| C. | 若生成1molSO3(s),放出热量大于$\frac{Q}{2}$ | |
| D. | 使用催化剂,改变反应途径,Q值也随之改变 |
 MgBr2
MgBr2
 氮化硼(BN)是新型无机非金属材料,可作润滑剂、高级耐火材料和超硬材料等,某兴趣小组以下装置用NH3与B2O3固体在高温下制备少量氮化硼.
氮化硼(BN)是新型无机非金属材料,可作润滑剂、高级耐火材料和超硬材料等,某兴趣小组以下装置用NH3与B2O3固体在高温下制备少量氮化硼.