题目内容
8.己知某温度下,Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1.12×10-12,下列叙述正确的是( )| A. | 向氯化银的浊液中加入氯化钠溶液,氯化银的溶解度减小 | |
| B. | 向2.0×10-1mol/L的K2CrO4溶液中加入等体积的2.0×10-1mol/LAgNO3溶液,则有Ag2CrO4沉淀生成 | |
| C. | 将一定量的AgCl和Ag2CrO4固体棍合物溶于蒸馏水中,充分溶解后,静置,上层清液中Cl-的物质的量浓度最大 | |
| D. | 将0.001 mol/L的AgNO3溶液滴入0.001mol/L的KCl和0.001 mol/L的K2CrO4溶液,则先产生AgCl沉淀 |
分析 A、据AgCl的Ksp分析,加入NaCl,氯离子浓度增大,AgCl溶解度减小;
B、计算溶液中的Q与Ksp(Ag2CrO4)=1.12×10-12 mol3•L-3比较;
C、AgCl和Ag2CrO4固体混合物溶于蒸馏水中,AgCl和Ag2CrO4都会产生银离子;
D、根据Ksp(AgCl)、Ksp(Ag2CrO4),计算Cl-、CrO42-开始沉淀时c(Ag+),需要c(Ag+)小的先沉淀.
解答 解:A、向氯化银的浊液中加入氯化钠溶液,氯离子浓度增大,沉淀的溶解平衡逆向移动,AgCl溶解度减小,故A正确;
B、Q=c2(Ag+)×c(CrO42-)=$(\frac{2.0×1{0}^{-4}}{2})^{2}×(\frac{2.0×1{0}^{-4}}{2})$=1.0×10-12<Ksp(Ag2CrO4)=1.12×10-12 mol3•L-3,所以没有沉淀生成,故B错误;
C、AgCl和Ag2CrO4固体混合物溶于蒸馏水中,AgCl和Ag2CrO4都会产生银离子,所以银离子浓度最大,故C错误;
D、由Ksp(AgCl)、Ksp(Ag2CrO4),则当Cl-开始沉淀时c(Ag+)=$\frac{Ksp(AgCl)}{c(C{l}^{-})}$=1.56×10-10mol/L,当CrO42-开始沉淀时c(Ag+)=$\sqrt{\frac{Ksp(A{g}_{2}Cr{O}_{4})}{c(Cr{{O}_{4}}^{2-})}}$=4.36×10-5 mol/L,故先产生AgCl沉淀,故D正确;
故选AD.
点评 本题考查溶度积常数的有关计算、判断离子是否完全,沉淀等问题,综合性强,难度较大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.P和O2放在两容器中,控制不同条件,分别发生:4P+3O2=2P2O3(容器1),4P+5O2=P2O5(容器2),若在两容器中分别放1mol P和1molO2,充分反应后得到P2O3和P2O5的物质的量之比是( )
| A. | 1:1 | B. | 5:4 | C. | 4:3 | D. | 5:3 |
13.以硼镁矿( 2MgO.B2O3.H2O、SiO2及少量Fe3O4、CaCO3、Al2O3 )为原料生产硼酸的工艺流程如下:

已知:表一:不同温度下H3BO3的溶解度
表二:不同物质沉淀完全时的pH
(1)由于矿粉中含CaCO3,“浸取”时容易产生大量泡沫使物料从反应器中溢出,应采取的措施为应分批加入H2SO4 .
(2)“浸出液”显酸性,含有H3BO3、Mg2+和SO42-,还含有Fe2+、Fe3+、Ca2+、Al3+等杂质.“除杂”时,向浸出液中依次加入适量目H2O2和MgO,可以除去的杂质离子为Fe3+、Fe2+、Al3+,的作用为H2O2+2H++2Fe2+=2Fe3++2H2O(用离子方程式表示).
(3)“浸取”后,采用“热过滤”的目的为防止温度下降时H3BO3从溶液中析出.
(4)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图所示,且溶液的沸点随压强增大而升高.为了从“母液”中充分回收 MgSO4.H2O,应采取的措施是将“母液”蒸发浓缩,加压升温结晶.

(5)已知25℃时,硼酸( H3BO3)溶液中存在如下平衡:HBO3(aq)+H2O(l)?[B(OH)4]-(aq)+H+(aq) K=5.7×10-10;25℃时,0.7mol.L-1硼酸溶液中c(H)+≈2×10-5mol.L-1
(6)已知25℃时:
下列说法正确的是BD(填选项字母).
A.碳酸钠溶液滴入硼酸溶液中能观察到有气泡产生
B.碳酸钠溶液滴入醋酸溶液中能观察到有气泡产生
C.等浓度碳酸溶液和硼酸溶液的pH:前者>后者
D.等浓度碳酸钠溶液和醋酸钠溶液的pH:前者>后者.

已知:表一:不同温度下H3BO3的溶解度
| 温度℃) | 20 | 40 | 60 | 100 |
| 溶解度(g) | 5.0 | 8.7 | 14.8 | 40.2 |
| 物质 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| pH | 3.2 | 5.2 | 9.7 | 12.4 |
(2)“浸出液”显酸性,含有H3BO3、Mg2+和SO42-,还含有Fe2+、Fe3+、Ca2+、Al3+等杂质.“除杂”时,向浸出液中依次加入适量目H2O2和MgO,可以除去的杂质离子为Fe3+、Fe2+、Al3+,的作用为H2O2+2H++2Fe2+=2Fe3++2H2O(用离子方程式表示).
(3)“浸取”后,采用“热过滤”的目的为防止温度下降时H3BO3从溶液中析出.
(4)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图所示,且溶液的沸点随压强增大而升高.为了从“母液”中充分回收 MgSO4.H2O,应采取的措施是将“母液”蒸发浓缩,加压升温结晶.

(5)已知25℃时,硼酸( H3BO3)溶液中存在如下平衡:HBO3(aq)+H2O(l)?[B(OH)4]-(aq)+H+(aq) K=5.7×10-10;25℃时,0.7mol.L-1硼酸溶液中c(H)+≈2×10-5mol.L-1
(6)已知25℃时:
| 化学式 | H2CO3 | CH3COOH |
| 电离常数 | K1=4.4×10-7 K2=4.7×10-11 | K=1.75×10-5 |
A.碳酸钠溶液滴入硼酸溶液中能观察到有气泡产生
B.碳酸钠溶液滴入醋酸溶液中能观察到有气泡产生
C.等浓度碳酸溶液和硼酸溶液的pH:前者>后者
D.等浓度碳酸钠溶液和醋酸钠溶液的pH:前者>后者.
 3-甲基戊烷
3-甲基戊烷 2,2,3-三甲基丁烷
2,2,3-三甲基丁烷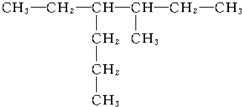 3-甲基-4-乙基庚烷
3-甲基-4-乙基庚烷 2,5-二甲基-3-乙基戊烷
2,5-二甲基-3-乙基戊烷 3,4-二甲基-5-乙基辛烷
3,4-二甲基-5-乙基辛烷 3-甲基-4-乙基己烷.
3-甲基-4-乙基己烷.
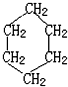 .
.